【2015年广东省】现有10%的Na2CO3溶液,请按下面要求计算:
(1)106 g上述溶液中所含溶质量为 g;
(2)106 g 上述溶液与足量10%的盐酸反应,最多可生成CO2多少克?
(3)向106 g 上述溶液中逐滴加入10%的盐酸并不断搅拌,此时发生的反应为:Na2CO3 + HCl =NaHCO3 + NaCl ;当Na2CO3 全部转化为NaHCO3后,再加入盐酸才开始放出CO2 。请在“题25图”中画出产生气体的曲线。

(4)另取10% Na2CO3溶液边搅拌边加入10%的盐酸,有关反应物与生成物的量如下表:
| 物质 |
Na2CO3 |
HCl |
X |
NaCl |
CO2 |
H2O |
| 质量/g |
31.8 |
14.6 |
16.8 |
23.4 |
4.4 |
m |
则m= ;该反应的化学方程式为 。
碳酸氢钠常用于食品和医药工业,某化学兴趣小组对碳酸氢钠进行探究。
【查阅资料】 Ⅰ.碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质。
Ⅱ.碳酸钠溶液呈碱性。
【进行实验】为了验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠到铜片上加热,如图所示。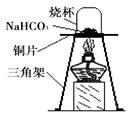
(1)加热一段时间后,观察到烧杯内壁有__________。
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊。写出该反应的化学方程式:___________________。
(3)兴趣小组的同学认为:充分加热后的固体产物可能是NaOH或Na2CO3。
①他们的依据是____________________________________。
②兴趣小组为了确定反应后的固体产物成分进行以下实验,请填写下表:
| 实验 |
实验现象 |
结论 |
| 实验一:取少量反应后的固体产物溶于水,滴入几滴酚酞试液 |
溶液变成红色 |
固体产物是NaOH,而不是Na2CO3 |
| 实验二:取少量反应后的固体产物溶于水,加入氯化钙溶液 |
_____________ |
固体产物是Na2CO3,而不是NaOH |
| 实验三:___________________ ___________________________ |
产生大量气泡 |
固体产物是Na2CO3,而不是NaOH |
【讨论与评价】实验一的结论与实验二、实验三的结论相反,在讨论时兴趣小组的同学认为方案一的结论不正确,他们的理由是_____________________________________________。
【总结】请写出碳酸氢钠受热分解的化学方程式________________________。
(4)某碱厂的主要产品之一是小苏打(碳酸氢钠),为了测定产品中碳酸氢钠的质量分数(假设该样品中只含氯化钠一种杂质),取样品10.0 g逐滴加入稀盐酸,所得气体的质量为4.4 g。求:样品中碳酸氢钠的质量分数。
现有 100 t含氧化铁80%的赤铁矿石,工业上用于冶炼生铁
(1)生铁主要是铁和的合金;
(2)100 t含氧化铁80%的赤铁矿石中氧化铁的质量=t ;
(3)用题中所给的赤铁矿石能冶炼出含杂质3%的生铁多少吨?
高温
(反应的化学方程式为Fe2O3 + 3CO ="2Fe" + 3CO2)
某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如图所示,请回答:
(1)当加入212g稀盐酸时,放出气体的质量为__________g
(2)碳酸钠样品中碳酸钠的质量分数为多少?(写出计算过程)
(3)加入106g稀盐酸(即A点)时烧杯中溶液溶质的质量分数为多少?(写出计算过程)
市场上有一种外观类似黄金的Cu—Zn合金 ,现取合金粉末20g放入烧杯中,加入50 g的稀硫酸,恰好完全反应,测得烧杯内剩余物的质量为69.8 g。求:
①产生氢气的质量;
②求出该合金中铜的质量分数;
③稀硫酸中溶质的质量分数;
④反应后所得溶液的溶质质量分数。
向碳酸钠和氯化钠的混合物15.6 g中加入100 g稀盐酸,恰好完全反应后,得到111.2 g溶液。试计算:
(1)产生二氧化碳多少克?
(2)所得溶液中溶质的质量分数是多少?