SO2和NO2都是大气污染物。
(1)将NO2变成无害的N2,要找到适合的物质G与适当的反应条件,G应为___________(填写“氧化剂”或“还原剂”).下式中X必须为无污染的物质,系数n可以为0.NO2+G N2+H2O+nX (未配平的反应式).下列化合物中,满足上述反应式中的G是________(填写字母)。
N2+H2O+nX (未配平的反应式).下列化合物中,满足上述反应式中的G是________(填写字母)。
a.NH3 b.CO2 c.SO2 d.CH3CH2OH
(2)采取还原法,用炭粉可将氮氧化物还原。
已知:N2(g)+O2(g)=2NO(g) △H=+180.6kJ•mol-1
C(s)+O2(g)=CO2(g) △H=-393.5kJ•mol-1
则反应C(s)+2NO(g)=CO2(g)+N2(g) △H="_____________" kJ•mol-1
(3)利用氨水可以将SO2和NO2吸收,原理如图1所示:NO2被NH4HSO3吸收的离子方程式是______________。浓度均为0.1mol/L的NH4HSO3溶液和NH4HSO4溶液中的c(NH4+)相比较,NH4HSO3_____________NH4HSO4。(选填“>”、“=”或“<”)
(4)利用图2所示装置(电极均为惰性电极)也可吸收SO2,并用阴极排出的溶液吸收NO2.
①b极的电极反应式为_________________________。
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32-生成.该反应离子方程式为________________________________。

(5)SO2也可用于消除铬的毒性。六价铬的毒性大约是三价铬的100倍,二氧化硫还原法是在酸性溶液中通SO2将Cr2O72-还原为Cr3+,然后再加碱将Cr3+沉淀,已知常温下Ksp[Cr(OH)3]=10-32,要使Cr3+沉淀完全(c(Cr3+)小于10-5mol/L),溶液的pH应升高到____________。
由环己烷可制备1,4环己醇二醋酸酯。下面是有关的8步反应(其中所有无机产物都已略去)。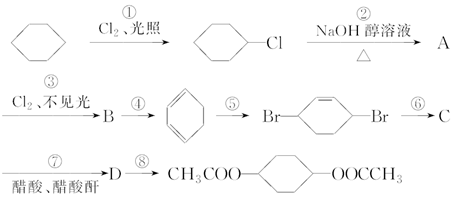
(1)在上述8步反应中,属于取代反应的有________,属于加成反应的有________,反应④属于________反应。
(2)写出下列化合物的结构简式。
B:________,C:________。
(3)写出反应④、⑤、⑥的化学方程式。
④____________________________________________________________,
⑤___________________________________________________________,
⑥__________________________________________________________。
(4)写出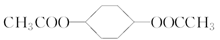 在NaOH溶液中水解的化学方程式:
在NaOH溶液中水解的化学方程式:
__________________________________________________________。
有机物A、B、C、D、E、F的转化关系如下:
已知:①A是芳香族化合物,其苯环上有2个对位取代基,均不含支链,遇FeCl3溶液能发生显色反应。
②F分子中除了2个苯环外,还含有一个六元环。
请回答下列问题:
(1)A中含氧官能团的名称是________,1 mol A与足量溴水反应最多可以消耗________mol Br2。
(2)反应①~③中属于加成反应的有________(填序号)。
(3)C的结构简式为________,F的结构简式为____________________。
(4)A→B的化学方程式是__________________________________________。
人们对苯及芳香烃的认识有一个不断深化的过程。已知分子式为C6H6的结构有多种,其中的两种为:
(Ⅰ) (Ⅱ)
(Ⅱ)
(1)这两种结构的区别表现在定性方面(即化学性质方面):Ⅱ能__________(填入编号,下同),而Ⅰ不能________。
| A.被酸性高锰酸钾溶液氧化 |
| B.与溴水发生加成反应 |
| C.与溴发生取代反应 |
| D.与氢气发生加成反应 |
定量方面(即消耗反应物的量的方面):1 mol C6H6与H2加成,Ⅰ需______mol,而Ⅱ需________mol。
(2)今发现C6H6还可能有另一种如图所示的立体结构,该结构的二氯代物有________种。
氧族元素(ⅥA族)的各种性质可归纳整理如下(部分):
| 元素 性质 |
8O |
16S |
34Se(硒) |
52Te(碲) |
| 单质沸 点(℃) |
-183 |
444.6 |
685 |
1 390 |
| 主要 化合价 |
-2 |
-2,+4, +6 |
-2,+4, +6 |
|
| 原子半 径(nm) |
0.074 |
0.102 |
0.116 |
0.143 |
| 单质与 H2反应 |
点燃易 化合 |
加热化合 |
加热 难化合 |
不能直 接化合 |
回答下列问题:
(1)氧原子的结构示意图为________,硫离子的结构示意图为________。
(2)碲的主要化合价可能有________。
(3)氧元素比硫元素的非金属性________(填“强”或“弱”)。请用化学方程式证明该结论:__________________________________________________________。
(4)H2O2被Cl2氧化生成O2,H2O2经常作脱氯剂,用于消除水中的Cl2,写出该反应的化学方程式:___________________。
如下表为元素周期表的一部分,请回答有关问题:
| ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
| 2 |
① |
② |
||||||
| 3 |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
||
| 4 |
⑨ |
⑩ |
(1)⑤和⑧的元素符号是________和________。
(2)表中最活泼的金属是________,非金属性最强的元素是________(填写元素符号)。
(3)表中能形成两性氢氧化物的元素是________,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物对应的水化物反应的化学方程式________________、_______________________。
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:_____________________________。