(每小题2分,共14分)某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
| A.在250mL的容量瓶中定容成250mL烧碱溶液; |
| B.用移液管移取25mL烧碱溶液于锥形瓶中并滴加几滴甲基橙指示剂; |
| C.在天平上准确称取烧碱样品Wg,在烧杯中加蒸馏水溶解; |
| D.将物质的量浓度为Mmol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始时的刻度数为V1mL; |
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点时消耗酸的体积为V2mL。
回答下列问题:
(1)正确的操作步骤的顺序是(用字母填写)
________→________→________→____D____→________;
(2)滴定管读数应注意 ___________________。
(3)操作E中在锥形瓶下垫一张白纸的作用是 _________________。
(4)操作D中液面应调整到 ,尖嘴部分应 。
(5)滴定终点时锥形瓶内溶液的pH约为 ,终点时溶液颜色的变化是 。
(6)若酸式滴定管没有用标准H2SO溶液润洗,会对测定结果有何影响? (填“偏高”、“偏低”或“无影响”)(其他操作均正确)。
(7)该烧碱样品的纯度计算式是 。
 1919年,Langmuir提出:原子数相同、电子数相同的分子,互称为等电子体。后来扩展为“等电子原理”,即等电子体的结构相似、物理性质相近。该原理常被用来发现或者合成具有特殊功能的晶体和有机物等诸多领域。如:X是一种新型无机材料,它与碳化硅(SiC)结构相似、物理性质相近,符合该原理。X有如下的转变:
1919年,Langmuir提出:原子数相同、电子数相同的分子,互称为等电子体。后来扩展为“等电子原理”,即等电子体的结构相似、物理性质相近。该原理常被用来发现或者合成具有特殊功能的晶体和有机物等诸多领域。如:X是一种新型无机材料,它与碳化硅(SiC)结构相似、物理性质相近,符合该原理。X有如下的转变:
其中:C是一种能使湿润的红色石蕊试纸变蓝的无色气体;D为白色沉淀且具有两性;E溶液的焰色反应中呈黄色火焰。回答以下问题:
(1)写出X的化学式:________,X属于________晶体(填“原子”、“分子”或“离子”)。
(2)写出X与A溶液反应的化学方程式:____________________ __________;
写出K与J反应的化学方程式:____________________________ _____。
|
(3)X与SiC的复合粉末是新一代大规模集成电路的理想散热材料。最近日本科学家研究出一种新物质与氮气制备该纳米级复合材料的方法,请将该反应补充完整(方框中填新物质的化学式)。+2N2 4X+SiC+3C。
4X+SiC+3C。
某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电便可制得有较强杀菌能力的消毒液,他设计了如图三套装置。
装置A(“能”或“不能”)用于消毒液发生器,简述理由;
用化学方程式表示装置B的反应原理:;上图装置哪一个更好?简述原因。
顺丁烯二酸二甲酯是一种重要的有机化工原料,广泛应用于涂料,油漆,杀虫剂尤其是在水处理剂等方面。下面是利用石油产品M合成顺丁烯二酸二甲酯的部分过程
|

化学兴趣小组同学运用类比学习的思想,探究过氧化钠与二氧化硫的反应。小组同学改进了右图所示的装置进行实验(已知制取SO2的反应为H2SO4+Na2SO3=Na2SO4+SO2↑+H2O)。充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃。试回答下列问题:
(1)请你完成装置改进的措施和理由:
①措施:在A、B之间加一个干燥管,
理由_____________________________;
②措施:_________________________________,
理由______________________________________。
(2)某同学推断该白色固体为Na2SO3,则其所类比的化学反应是_____________________(用化学方程式表示)。任何的推论都要经过检验,请完成对白色固体的探究:
限选实验仪器与试剂:烧杯、试管、药匙、滴管、酒精灯、试管夹;3 mol·L-1HCl、6 mol·L-1HNO3、NaOH稀溶液、蒸馏水、1 mol·L-1 BaCl2溶液。
①提出合理假设:
假设1: ;假设2: ;
假设3: ;
②设计实验方案证明你的假设,并按下表格式写出实验操作步骤、预期现象与结论。
| 实验操作 |
预期现象与结论 |
| 步骤1: |
|
| 步骤2: |
|
| … |
铝镁合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组为测定某含镁3%一5%的铝镁合金(不含其它元素)中镁的质量分数,设计以下实验方案进行探究。填写下列空白。
[实验方案]铝镁合金粉末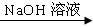 测定剩余固体质量
测定剩余固体质量
[实验步骤]
步骤1:称取5.4g铝镁合金粉末样品,投入VmL 2.0mol·L—1NaOH溶液中,充分反应。
步骤2:过滤、洗涤、干燥、称量固体。
[交流与讨论]
(1) 实验中发生反应的化学方程式是;
(2)参与反应的NaOH溶液的体积V≥;
(3)步骤2中,如果经两次过滤滤液仍浑浊,则原因可能是_________(只填一点);
(4)步骤2中,若未洗涤固体,测得镁的质量分数将(填“偏高”或“偏低”)。
[实验拓展] 请你另设计一个实验方案(用上述方案的试剂),测定该铝镁合金中镁的质量分数。
要求:从下图中挑选所需的仪器,画出该方案的实验装置简图(添加必要的塞子、玻璃导管、胶皮管,固定装置不用画),并标明所用试剂.