常温下,将Cl2缓慢通入水中至饱和,然后向其中滴加0.1mol/LNaOH溶液。整个实验过程中溶液的pH变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是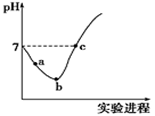
| A.实验过程中用pH试纸测定溶液的pH |
| B.a~b段,溶液中 C(H+)/C(OH-) 减小 |
| C.b点对应溶液中:c(Cl-)>c(H+)>c(HClO)>c(ClO-)>c(OH-) |
| D.c点对应溶液中:c(Na+)=c(Cl-)+c(ClO-) |
“单质 → 氧化物 → 酸或碱 →盐”,以下单质不能完成这种一步转化的是()
| A.硫 | B.碳 | C.铜 | D.钙 |
在一定温度和压强下,1体积X2气体与3体积Y2气体化合生成2体积气体化合物,则该化合物的化学式为()
| A.XY3 | B.XY | C.X3Y | D.X2Y3 |
含有相同分子数的下列物质,质量最小的是()
| A.O2 | B.CH4 | C.CO2 | D.SO2 |
如果4g甲烷含有的分子数为a个,则阿伏加德罗常数用含a的代数式可表示为()
| A.a mol-1 | B.0.25amol-1 | C.2amol-1 | D.4amol-1 |
已知3.01×1023个X气体分子的质量为16g,则X气体的摩尔质量是()
| A.16g | B.32g | C.64g /mol | D.32g /mol |