读某日我国四城市正午太阳高度示意图,完成各题。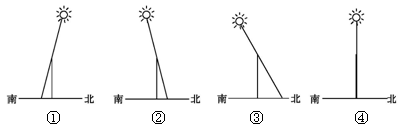
若四城市为广州、武汉、北京、海口市,则图中①②③④分别代表的城市为
| A.海口、武汉、北京、广州 | B.武汉、北京、广州、海口 |
| C.海口、北京、武汉、广州 | D.广州、武汉、北京、海口 |
据图判断,此时我国最有可能处于二十四节气中的
A.春分 B.夏至 C秋分 D.冬至
2013年9月29日,我国大陆境内的第一个自贸区——上海自由贸易试验区正式挂牌成立,之后许多跨国公司总部纷纷落户上海自贸区。图为“上海城市空间形态示意图”读图完成各题。
吸引跨国公司总部落户上海自贸区的最主要因素是
| A.交通 | B.政策 |
| C.技术 | D.市场 |
图中的上海磁悬浮列车专线(龙阳路站至浦东国际机场)是世界第一条商业运营的磁悬浮专线,它带来的影响可能是
| A.中心商务区将移至郊区 |
| B.沿线地带形成大型工业区 |
| C.中心城区辐射作用增强 |
| D.城市其他交通运输方式衰落 |
图为“我国目前部分优势商品粮基地分布和粮食流通方向示意图”。读图完成各题。
关于甲、乙、丙、丁商品粮基地优势条件和限制性条件叙述正确的是
| A.甲地人均耕地多,热量不足 |
| B.乙地夏季降水充足,光热不足 |
| C.丙地水源充足,地形崎岖 |
| D.丁地光、热、水充足,旱涝灾害频发 |
M地区曾经是全国重要的商品粮基地,目前其地位有所下降,主要原因有
 ①水利工程的建设缓慢②农业劳动力严重流失
①水利工程的建设缓慢②农业劳动力严重流失
③城市化发展快,非农用地增多 ④农业结构调整,粮食种植面积减少
| A.①④ | B.②③ | C.③④ | D.①② |
图为“某城镇略图”,读图完成各题。
图中①②③所代表的城市功能区分别是
| A.住宅区、工业区、商业区 |
| B.工业区、住宅区、商业区 |
| C.商业区、住宅区、工业区 |
| D.住宅区、商业区、工业区 |
若乙处为新开楼盘,下列房地产开发商的广告词中,能反映其自然优美环境的是
| A.毗邻大学,文化氛围浓厚 | B.交通便利,四通八达 |
| C.视野开阔,俯瞰全城 | D.绝版水岸名邸,依山傍水 |
2013年11月我国开始启动“单独二孩”政策,即夫妻双方一人为独生子女,第一胎非多胞胎,即可生二胎。据此完成各题。
启动此项政策的国情是我国
| A.人口死亡率增高 | B.人口老龄化加剧 |
| C.环境承载力提高 | D.人口出现负增长 |
20.到2030年,此项政策将使我国
| A.就学与就业压力减轻 | B.养老金支付总额减少 |
| C.劳动力人口减幅放缓 | D.男多女少的情况加剧 |
2013年11月13世界气候大会在波兰华沙开幕,会议推动各国政府在2015年达成一个全球性气候协议的道路上更进了一步,包括一些重要的新决议,通过保护森林、节能和灾害预防等措施减少二氧化碳排放。图为“世界部分国家二氧化碳排放总量和人均排放量图”读图完成各题。
有关二氧化碳排放叙述正确的是
| A.人口大国的人均碳排放量大 | B.发达国家的人均碳排量较大 |
| C.城市化速度与碳排量呈正相关 | D.各国应承担同等的碳排放责任 |
当前我国应采取的二氧化碳减排措施主要是
①开展植树造林②减缓工业化进程③提高能源利用效率④开发新能源
| A.①② | B.①③ | C.②④ | D.③④ |