下列有关物质性质、用途说法正确的是
| A.乙醇、次氯酸钠溶液均可将病毒氧化而达到消毒目的 |
| B.晶体SiO2可以导电,因而可用作光导纤维· |
| C.为了增强去污能力,可将洁厕灵(主要成分为盐酸)与84消毒液(主要成分为次氯酸钠)混用 |
| D.氯水和明矾都可用作水处理剂,二者作用原理不同 |
在一个0.5L密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和5.4 mol·L-1,在一定的条件下发生反应N2(g) + 3H2(g) 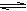 2NH3(g)。10min后测得N2的浓度是0.8 mol·L-1,则在这10min内NH3的平均反应速率是
2NH3(g)。10min后测得N2的浓度是0.8 mol·L-1,则在这10min内NH3的平均反应速率是
| A.0.1mol·L-1·min-1 | B.0.6mol·L-1·min-1 |
| C.0.3mol·L-1·min-1 | D.0.2mol·L-1·min-1 |
实验室用3.0 mol·L-1的硫酸溶液与锌粒反应制取氢气。下列措施中可能加大反应速率的是
| A.适当降低温度 | B.将锌粒改为锌粉 |
| C.将所用硫酸换成98%的浓硫酸 | D.加入少量醋酸钠固体 |
影响化学反应速率的因素很多,下列措施肯定不能加快化学反应速率的是
| A.降低温度 | B.升高温度 | C.使用催化剂 | D.增加反应物浓度 |
下列各图中,表示正反应是吸热反应的图是
下列说法正确的是
| A.反应条件是加热的反应都是吸热反应 |
| B.化学反应除了生成新的物质外,还伴随着能量的变化 |
| C.物质燃烧不一定是放热反应 |
| D.放热的化学反应不需要加热就能发生 |