甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数。下列判断正确的是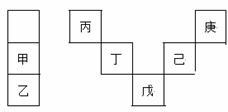
| A.丙与戊的原子序数相差28 |
| B.气态氢化物的稳定性:庚<己<戊 |
| C.常温下,甲和乙的单质均能与水剧烈反应 |
| D.丁的最高价氧化物不与任何酸反应 |
常温下分别将下列各组中的两种溶液等体积混合,所得溶液的pH一定等于7的是
| A.0.1mol/L的某一元酸和0.1mol/L的某一元碱 |
| B.0.1mol/L的某二元强酸和0.1mol/L的某二元碱 |
| C.pH=2的某一元酸和pH=12的某一元碱 |
| D.pH=3的某二元强酸和pH=11的某一元强碱 |
下列各组离子可能大量共存的是
| A.pH=1的溶液中:Fe2+、A13+、Cl-、MnO4- |
| B.能与金属铝反应放出氢气的溶液:K+、NO3-、Cl-、NH4+ |
| C.能使酚酞试液变红的溶液中:Na+、Cl-、S2-、SO32- |
| D.常温下c(OH-)/c(H+)=1012的溶液中:K+、Mg2+、Cl-、Br- |
NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.标准状况下,11.2 L NO和11.2 L O2混合后气体的分子总数为0.75NA |
| B.室温下,42.0g乙烯和丙烯的混合气体中含有的碳原子数为3NA |
| C.常温下,pH=2的稀盐酸中所含有的H+离子数大于0.01 NA |
| D.1mol CH3+(碳正离子)中含有电子数为10NA |
下列离子方程式正确的是
A.氯化铝溶液水解显酸性:Al3++3H2O Al(OH)3↓+3H+ Al(OH)3↓+3H+ |
| B.向漂白粉溶液中通入SO2气体:Ca2++2C1O-+SO2 +H2O= CaSO3↓+2HC1O |
C.用石墨作电极电解CuCl2溶液:2C1-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| D.含有等物质的量的氢氧化钡、明矾两种溶液混合: |
3Ba2++6OH-+2A13++3SO42-=3BaSO4↓+2Al(OH)3↓[
下列关于溶液和胶体的叙述,错误的有
①直径介于1 nm ~ 100 nm之间的微粒称为胶体②溶液是电中性的,胶体是带电的
③.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动.
④用含1 mol FeCl3的溶液可制得6.02×1023个Fe(OH)3胶体粒子
| A.1个 | B.2个 | C.3个 | D.4个 |