向质量分数为2a%,体积为10 mL,物质的量浓度为c1 mol·L-1的稀H2SO4中加入V mL 的水,使之质量分数变为 a%,此时物质的量浓度为c2 mol·L-1,则下列关系正确的是
| A.V>10, 2c2=c1 | B.V<10,2c2﹤c1 |
| C.V>10,2c2<c1 | D.V>10, 2c2>c1 |
国际化学年的主题是“化学—我们的生活,我们的未来”。下列说法不正确的是
| A.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物。PM2.5被吸入人体后会直接进入支气管,易引发包括哮喘、支气管炎和心血管病等方面的疾病 |
| B.推广使用应用原电池原理制成的太阳能电池和氢动力汽车,减少化石能源的使用 |
| C.利用二氧化碳等原料合成的聚碳酸酯类可降解塑料替代聚乙烯塑料 |
| D.生物柴油的主要成分是利用从泔水中提取的地沟油与甲醇反应生成的脂肪酸甲酯类化合物,与石化柴油有本质不同 |
食盐晶体如图所示。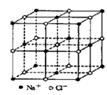
在晶体中·表示Na+,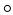 表示Cl-,已知食盐的密度为ρg/cm3,NaCl摩尔质量是Mg/mol,阿伏伽德罗常数为N,则在食盐晶体中Na+和Cl-的距离大约是
表示Cl-,已知食盐的密度为ρg/cm3,NaCl摩尔质量是Mg/mol,阿伏伽德罗常数为N,则在食盐晶体中Na+和Cl-的距离大约是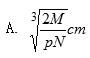
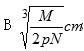
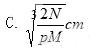
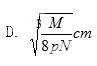
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.17g羟基(-OH)所含有的电子数是10 NA个 |
| B.1mol苯乙烯中含有的碳、碳双键数为4NA个 |
| C.常温下,14g乙烯和丙烯的混合物中总原子数为3NA个 |
| D.4.2g C3H6中含有的碳碳双键数一定为0.1NA |
下列物质中,属于酸性氧化物但不溶于水的是
| A.Al2O3 | B.CO2 | C.SO3 | D.SiO2 |
下列反应中,氧化剂与还原剂物质的量的关系为1:2的是
| A.4KI+O2+2H2O=4KOH+2I2 |
| B.2CH3COOH+Ca(ClO)2=2HClO+(CH3COO)2 Ca |
| C.I2+2NaClO3=2NaIO3+Cl2 |
D.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O MnCl2+Cl2↑+2H2O |