某校化学探究小组成员讨论下列Ⅰ、Ⅱ、Ⅲ、Ⅳ四种仪器装置的气体制备与性质实验的用法,其中不合理的是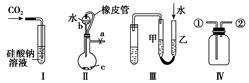
| A.装置Ⅰ:可以用来验证碳的非金属性比硅强 |
| B.装置Ⅱ:橡皮管的作用是使水顺利流下 |
| C.装置Ⅲ:不能检查该装置的气密性 |
| D.装置Ⅳ:先从①口进气收集满二氧化碳,再从②口进气,可收集NO气体 |
下列各组中的两种有机物,其最简式相同但既不是同系物,又不是同分异构体的是
| A.苯苯乙烯 | B.甲醛乙二醛 |
| C.对甲基苯酚苯甲醇 | D.甲酸乙醛 |
下列属于物理变化的是
| A.重油的裂化 | B.硝酸使蛋白质变性 |
| C.煤的干馏 | D.石油的分馏 |
下列叙述正确的是
①用植物纤维制造出的机动车燃料,属清洁的可再生能源
②用甲醛溶液浸泡海产品,使海产品保鲜
③变质的油脂有难闻的刺激性气味,是由于油脂发生了水解反应
④蜂蚁叮咬人的皮肤时将分泌物注入人体,此时可在患处涂抹小苏打溶液或稀氨水
⑤提倡在生活中不用塑料袋,是为了防止白色污染
| A.①④⑤ | B.②③④ | C.①③⑤ | D.①②③④⑤ |
在物质结构研究的历史上,通过α粒子散射实验,提出原子结构有核模型的是:
| A.道尔顿 | B.卢瑟福 | C.汤姆生 | D.波尔 |
主链含5个碳原子,有甲基、乙基2个支链的烷烃有
| A.2种 | B.3种 | C.4种 | D.5种 |