根据下列装置,结合所学化学知识回答下列问题:
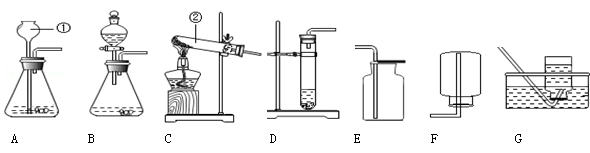
(1)写出图中标号仪器的名称:① ;② ;
(2)实验室用双氧水和二氧化锰制取少量纯净的氧气时,收集装置(填字母,下同)选用 ,能用此收集方法的原因是 ,如需随时控制反应速率并节约药品,发生装置最好选用 ,二氧化锰是该反应的 。
(3)实验室用高锰酸钾制取氧气时,发生装置应选用 (填字母);其反应的文字表达式是 ,二氧化锰是该反应的 物。用氯酸钾制氧气的文字表达式
(4)如用G装置收集氧气,开始收集的最佳时刻是 ,判断氧气是否收集满的现象是 ,实验结束后发现水槽中的水变红了,可能的原因是 。
(5)氨气极易溶于水,且密度比空气小,实验室常用加热固体硫酸铵和固体熟石灰的混合物来制取氨气,应用 装置,收集氨气最好用 装置。
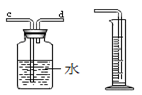
(6)为了测量生成氧气的体积可用右图装置,氧气从________________端进入(填序号),可从____________得出氧气的体积.测量体积时应当气泡____________(填“刚一冒出”或“连续均匀冒出”)时开始收集,因为装置内空气对测量体积_____________(填“有影响”或“无影响”)
(1)用下列物质的序号填空:
①碳酸钙②氢氧化钠③氧化钙④碳酸氢钠⑤熟石灰⑥稀盐酸
常用作食品干燥剂的是; 常用作补钙剂的是;
可用于改良酸性土壤的是; 可用于金属表面除锈的是;
常用作发酵粉和治疗胃酸过多的是;
用于肥皂、石油、造纸、纺织、印染等工业的碱是。
(2)硒被誉为“抗癌大王”。根据下图提供的有关硒的信息填空:
硒(Se)属于(填“金属”或 “非金属”)元素, 其相对原子质量为,在化学反应中, 硒原子容易(填“得到”或“失去”)电子形成硒离子(写离子符号)。
归纳与演绎是重要的科学方法,也是常用的化学学习方法。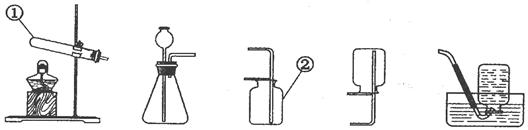
A B C D E
(1)写出标号仪器的名称:①、②;
(2)我们已经学过实验室制取O2、H2、CO2三种气体的反应原理,制取与收集方法,请你归纳出实验室制取这三种气体反应的共同点(填序号)。
| A.需要加热 | B.需用催化剂 | C.没有气体参加反应 | D.生成的气体只有一种 |
(3)气体发生装置_________可用来制取CO2,可采用装置来收集该气体。(填序号)
(4)实验室制取某气体时,E装置中的水变成了紫红色。则该同学选择的是__________发生装置(填序号),发生该现象的可能原因是___________________________________。
有一包白色固体,可能由氯化钠、硫酸铜、氯化钡、硝酸钠、碳酸钠、硫酸钠中的一种或几种组成,进行如下实验:①将粉末溶于水,得到白色沉淀和无色滤液;②过滤,在白色沉淀中加入稀硝酸,沉淀一部分消失,并生成气泡;③在滤液中加入硝酸银溶液,生成白色沉淀,加稀硝酸,沉淀不消失。则原液中一定有。一定没有。可能有的为。
②中的反应方程式为。
在置换反应:A+B→C+D中,
(1)若D为氢气,B为稀硫酸,则A的选择应满足的条件是;
(2)若D为铜,化合物B的物质类别可能为; (选填“氧化物”、“酸”、“碱”或“盐”)
(3)某些非金属也有活动性顺序。已知在溶液中可发生下列反应:Cl2+2NaBr=2NaCl+Br2,Br2+2NaI=2NaBr+I2,则在Cl2、Br2、I2三种非金属中,活动性最强的是,活动性最弱的是。
(1)在H、O、C、Cl、Na、Ca六种元素中选择适当元素,组成符合下列要求的物质,将其中化学式填入空格中。
①人工降雨的氧化物;
②可用于金属表面除锈的酸;
③可用作发酵粉和治疗胃酸过多症的是;
④可做建筑材料的盐;
(2)人的胃液中含有少量的盐酸。按要求将有关的化学方程式填写在横线上。
①胃酸过多时,常服用含有氢氧化铝的药物,其作用是___________________________。
②Ba2+有毒。用X射线检查胃病时常服用钡餐(硫酸钡),但误服碳酸钡可引起中毒,其中的原因为。
③误服碳酸钡中毒后可立即服用泻药(硫酸镁)来解毒,原因是。
(3)熊健同学到舅父家做客,看到一个化肥“蛇皮袋”上印有如图所示商标,还嗅到一股刺激性气味。熊健向舅父解释说:
①硝酸铵属于化肥中的(填序号)。
A.钾肥 B.氮肥 C.磷肥
每袋该化肥中含氮元素的质量至少为 kg。
②硝酸铵应具有的性质是(填序号)。
A.易溶于水 B.有挥发性 C.受热易分解
③硝酸铵能与强碱反应,其中与烧碱反应的反应方程式为:
NH4NO3 + NaOH = NaNO3 + NH3↑ + X。则X的化学式为;施用该类肥料时,要避免与(选填“酸”或“碱”)性物质混用,否则会降低肥效。