在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始状态均为c(A)=0.100 mol·L-1、c(B)=0.200 mol·L-1、c(C)=0 mol·L-1。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是
C分别在三种不同实验条件下进行,它们的起始状态均为c(A)=0.100 mol·L-1、c(B)=0.200 mol·L-1、c(C)=0 mol·L-1。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是
A.反应的平衡常数:①<②
B.反应A+2B C的ΔH>0
C的ΔH>0
C.实验②平衡时B的转化率为60%
D.实验③平衡时c(C)=0.040 mol·L-1
下列说法正确的是( )
| A.KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| B.25℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V(醋酸)<V(NaOH) |
| C.向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
| D.AgCl沉淀易转化成AgI沉淀且K(AgX)=c(Ag+)·c(X-),故K(AgI)<K(AgCl) |
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。已知: pM="-lg" c(M),pc(CO32-)=" -lg" cc(CO32-)。下列说法正确的是 ()
| A.MgCO3、CaCO3、MnCO3的Ksp依次增大 |
| B.a 点可表示MnCO3的饱和溶液,且c(Mn2+)= c(CO32-) |
| C.b 点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-) |
| D.c 点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32-) |
下列有关说法正确的是()
| A.反应NH3(g)+HCl(g)="==" NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
| B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极 |
C.CH3COOH 溶液加水稀释后,溶液中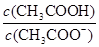 的值减小 的值减小 |
| D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
下列有关电解质溶液的说法正确的是()
| A.在蒸馏水中滴加浓H2SO4,KW不变 |
| B.CaCO3难溶于稀硫酸,也难溶于醋酸 |
| C.在Na2S稀溶液中,c(H+)=c(OH-)-2c(H2S)-c(HS-) |
| D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
右图表示溶液中c(H+)和c(OH-)的关系,下列判断错误的是()
| A.两条曲线间任意点均有c(H+)×c(OH-)=Kw |
| B.M区域内任意点均有c(H+)<c(OH-) |
| C.图中T1<T2 |
| D.XZ线上任意点均有pH=7 |