研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=_____________kJ·mol-1。
SO3(g)+NO(g)的ΔH=_____________kJ·mol-1。
一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是__________________。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K=____________。
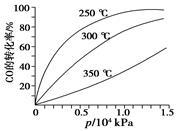
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH=_____________0(填“>”或“<”)。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH=_____________0(填“>”或“<”)。
实验室常用不含Fe3+的FeSO4溶液与NaOH溶液反应制备Fe(OH)2。
(1)用FeSO4晶体配制上述FeSO4溶液时还需加入来防止Fe2+被氧化,配制时所需的蒸馏水常采用的方法除去溶解的O2,检验所配FeSO4溶液中不含有Fe3+的最佳试剂是。
(2)Fe(OH)2露置在空气中容易被氧化,试写出该反应的化学方程式并用单线桥法表示该反应的电子转移情况;为防止Fe(OH)2氧化,实验时可在FeSO4溶液中加入适量的(选填“煤油”或“四氯化碳”)来隔绝空气。
按要求回答下列问题:
(1)O4是意大利的一位科学家合成的一种新型氧分子,一个分子由四个氧原子构成,在相同条件下,等质量的O4和O3氧原子数之比为;两种气体的体积之比为。
(2)已知下列几种物质①氨气②液氯③硫酸④盐酸⑤酒精⑥烧碱⑦氢氧化铁胶体,其中属于电解质的
是(填写序号)。
(3)硅是太阳能电池和电脑芯片不可缺少的材料。生产高纯硅的流程示意图如下:
物质A的化学式为;制备粗硅的反应为置换反应,且生成的气体具有还原性,该反应的化学方程式为 (提示:石英砂的主要成分是SiO2)。
实验室需要配制240mL 1.0 mol·L-1的NaOH溶液。试回答以下有关问题:
(1)该实验中至少需要称取氢氧化钠固体的质量为。
(2)该实验所需要的玻璃仪器,除烧杯、玻璃棒、量筒、胶头滴管外,还需要。
(3)烧碱溶解后未冷却至室温即转移定容,配得的溶液浓度将(填“偏大”、“偏小”或“无影响”,后同);定容时俯视刻度线,配得的溶液浓度将。
(1)造成水体污染的原因是。(填序号)
① 生活污水的任意排放② 工业废水的任意排放
(2)为了治理汽车尾气的污染问题,可以在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成CO2和N2,写出该反应的化学方程式:
_____。
(3)有机合成材料的出现是材料发展史上的一次重大突破。人们常说的三大合成
材料是指、和。
当前环境污染问题越来越严重,如酸雨、温室效应、臭氧层破坏、有毒物质的污染、汽车尾气的污染、水体污染等已成为世界各国普遍关注和研究的问题。
(1)引起温室效应的主要气体是(填序号,下同)。①SO2 ②CO2
(2)能形成酸雨的物质是。①硫的氧化物 ②碳的氧化物 ③氮的氧化物