氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+550 kJ·mol-1
它由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g) △H=+177 kJ·mol-1
ii.SO3(g)分解。
L(L1、L2)、X可分别代表压强和温度。下图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。
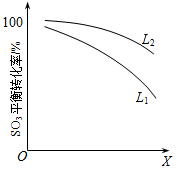
①X代表的物理量是 。
②判断L1、L2的大小关系,L1 L2
并简述理由: 。
某链烃A1mol,在一定条件下完全分解(裂解)成1mol烷烃B和1mol烯烃C,生成的混合气体对氢气的相对密度为14.5.通过计算回答下列问题:
⑴写出链烃A可能的结构简式和名称
⑵烷烃B和烯烃C可能各是什么?
⑶如果要求1molB完全燃烧时需要的氧气的物质的量是整数,那么C只能是什么烯烃?
以下是某同学写出的己烷同分异构体的结构简式,请判断是否有重复和遗漏现象。
为了测定甲烷的分子式,取一定量的甲烷置于一密闭容器中燃烧,定性实验表明产物是CO2、CO和水蒸气。学生甲、乙设计了两个方案,均认为根据自己的方案能求出甲烷的最简式。他们测得的有关数据如下(箭头表示气流的方向,实验前系统内的空气已排尽)。
(1)根据两方案,你认为能否求出甲烷的最简式?
(2)请根据你选择的方案,通过计算求出甲烷的最简式。
(3)丙同学认为若要单纯依靠这些数据,无法确定甲烷的分子式,你是否同意他的观点?说明理由。
小明从小爱吃鱼和瘦肉,不喜欢吃蔬菜水果。于是特别疼爱他的奶奶就将小明的一日三餐安排为:早餐:肉丝面;午餐:红烧鱼、排骨汤、大米饭;晚餐:瘦肉粥、炸鸡腿。请你评价一下小明奶奶的这种膳食安排是否合理,并说明你的依据。
食盐、醋作为食品添加剂有哪些作用?