下列说法或表示方法正确的是
| A.反应物总能量低于生成物总能量时,该反应不能发生 |
| B.强酸跟强碱反应放出的热量称为中和热 |
| C.由石墨比金刚石稳定可知,C(石墨,固)=C(金刚石,固)△H>O |
| D.在101kPa、25℃时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式表示为:2H2(g)十02(g)=2H2O(l);△H=-285.8KJ/mol |
在25mL 0.1mol·L-1NaOH溶液中逐滴加入0.2mol·L-1CH3COOH溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是
A.在A、B间任一点(不含A、B点),溶液中可能有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.在C点,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.在D点,c(CH3COO-)+c(CH3COOH)=c(Na+)
已知时,溶液的pH5.1,现用盐酸滴定20mL 氨水,用甲基橙作指示剂,达到终点时所用盐酸的量是
| A.10mL | B.5mL | C.大于10mL | D.小于5mL |
化学反应H2+Cl2===2HCl的能量变化如图所示,则下列说法正确的是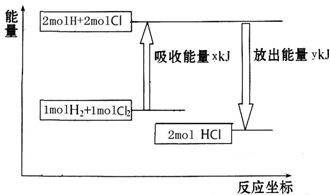
| A.该反应是放热反应 |
| B.断裂1 mol H—H键和1 mol Cl—Cl 键放出x kJ能量 |
| C.断裂1 mol H—Cl键需要吸收y kJ的能量 |
| D.2 mol HCl的总能量高于1 mol H2和1 molCl2的总能量 |
X、Y、Z是三种常见元素的单质,甲乙是两种常见的化合物,这些单质和化合物之间存在如图所示的关系,下列说法正确的是
| A.X、Y、Z都是非金属单质 |
| B.X、Y、Z中至少有一种是金属单质 |
| C.如果X、Y都为非金属单质,则Z必为金属单质 |
| D.如果X、Y都为金属单质,则Z必为非金属单质 |
下列说法中错误的是
| A.燃烧一定是氧化还原反应 | B.燃烧一定会放出热量 |
| C.燃烧一定有氧气参加 | D.燃烧一定伴有发光现象 |