用NA表示阿伏加德罗常数,下列叙述正确的是
| A.l mol甲基(-CH3)含有9 NA个电子 |
| B.标准状况下,22.4 L SO3含有的原子数为4NA |
| C.0.10 mol·L-1NaOH溶液中含有OH-离子数是0.1NA |
| D.5.6 g Fe与2.24 L Cl2充分反应转移电子数为0.2NA |
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表: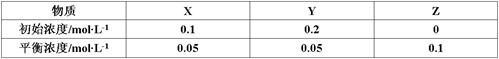
下列说法错误的是
| A.反应达到平衡时,X的转化率为50% |
B.反应可表示为X+3Y 2Z,其平衡常数为1600 2Z,其平衡常数为1600 |
| C.增大压强使平衡向生成Z的方向移动,平衡常数增大 |
| D.改变温度可以改变此反应的平衡常数 |
已知室温时,0.1mo1•L-1某一元酸HA在水中有0.1%发生电离,下列叙述错误的是
| A.该溶液的pH=4 |
| B.升高温度,溶液的pH增大 |
| C.此酸的电离平衡常数约为1×10-7 |
| D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
下列关于催化剂的说法不正确的是
| A.温度越高,催化剂的催化效果越好 |
| B.汽车排气管上的“催化转化器”能减少有害气体排放 |
| C.催化剂可以改变化学反应速率,但反应前后质量和化学性质不变 |
| D.锌与盐酸反应时,加入几滴硫酸铜溶液可加快反应速率,但硫酸铜不作催化剂 |
关于pH相同的醋酸和盐酸溶液,下列叙述不正确的是
| A.取等体积的两种酸溶液分别稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m>n |
| B.取等体积的两种酸溶液分别与完全一样的足量锌粒反应,开始时反应速率盐酸大于醋酸 |
| C.取等体积的两种酸溶液分别中和NaOH溶液,醋酸消耗NaOH的物质的量比盐酸多 |
| D.两种酸溶液中c(CH3COO-)=c(Cl-) |
氢氧燃料电池以氢气作还原剂,氧气作氧化剂,电极为多孔镍,电解质溶液为30%的氢氧化钾溶液。以下有数种说法:
①负极反应为O2+2H2O+4e―→4OH―;
②负极反应为2H2+4OH――4e―→4H2O;
③电池工作时正极区pH升高,负极区pH下降;
④电池工作时溶液中的阴离子移向正极。
正确的组合是
| A.②③ | B.②④ | C. ①③④ ①③④ |
D.①④ |