(15分) 铝铁合金在微电机中有广泛应用,某兴趣小组为利用废弃的铝铁合金设计了如下实验流程制备聚合硫酸铁和明矾:

(1)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是 。
②有人认为上述流程中的“氧化”设计存在缺陷,请提出改进意见: ;浓缩时向其中加入一定量的乙醇,加入乙醇的目的是 。
③加入试剂Y的目的是调节pH,所加试剂Y为 ;溶液的pH对[Fe2(OH) x(SO4)y]n中x的值有较大影响(如图1所示),试分析pH过小(pH<3)导致聚合硫酸铁中x的值减小的原因: 。

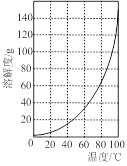
图1 图2
(2)明矾是一种常见铝钾硫酸盐。
①为充分利用原料, 试剂X应为 。
②请结合图2所示的明矾溶解度曲线,补充完整由滤液Ⅰ制备明矾晶体的实验步骤(可选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):向滤液Ⅰ中加入足量的含铝废铁屑至不再有气泡产生, ,得到明矾晶体。
W、X、Y、Z为短周期内除稀有气体外的4种元素,它们的原子序数依次增大,其中W是原子序数最小的元素,只有Y为金属元素。Y和W的最外层电子数相等。Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍。由此可知:
(1)写出元素符号:W为 ,X为 , Y为 ,Z为 。
(2)W2Z是由 键组成的分子,其电子式为 。
(3)由Y、X、W组成的物质中有 键和 键组成的 化合物。
下列结构图中,●代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表代价键(示例F2):  。
。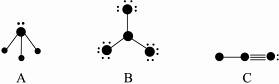
根据各图表示的结构特点,写出各分子的化学式:
A ,B ,C 。
下列五种物质中①Ar②CO2③SiO2④NaOH⑤K2S,只存在共价键的是___________,只存在离子键的是___________,既存在离子键又存在共价键的是___________,不存在化学键的是___________。(填序号)
由A、B元素组成的含4个原子核和42个电子的-2价阳离子中,1个A的核内质子数比B的核内质子数多8个,试通过计算确定:
(1)A、B元素名称分别为和。
(2)写出该阴离子的离子符号。
(3)该阴离子与钠离子形成的化合物中含有键。
A、B、C、D、E是中学化学常见的分子或离子,它们具有相同的电子数,且A是由5个原子核组成的粒子。它们之间可发生如下变化,且D与酸性氧化物、碱性氧化物均能反应。
A+B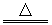 C+D B+E====2D
C+D B+E====2D
(1)写出A的电子式______________。
(2)写出B的化学式______________。
(3)写出D的电子式______________。