下列离子方程式正确的是
| A.向NaHSO4溶液中滴加过量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| B.用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32- |
| C.将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O |
| D.向碳酸氢钠溶液中加入氢氧化钠:HCO3-+ OH-=CO2↑+H2O |
常温下,将甲酸与NaOH溶液混合,所得溶液的pH=7,则此溶液中()
| A.c(HCOO-)>c(Na+) |
| B.c(HCOO-)<c(Na+) |
| C.c(HCOO-)= c(Na+) |
| D.无法确定c(HCOO-)与c(Na+)的关系 |
25℃时,将稀氨水逐滴滴加到稀硫酸中,当溶液的pH=7时,下列关系正确的是()
| A.c(NH4+)=c(SO42-) |
| B.c(NH4+)>c(SO42-) |
| C.c(NH4+)<c(SO42-) |
| D.c(NH4+)+c(SO42-)= c(H+)=c(NH4+) |
有机物A的结构简式如右图所示,下列有关该物质的说法正确的是: 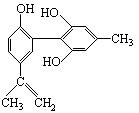
| A.遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 |
| B.滴入酸性KMnO4溶液,观察紫色褪去,能证明结构中存在碳碳双键 |
| C.1 mol该物质分别与浓溴水和H2反应时,最多消耗Br2 和H2分别为4 mol、7 mol |
| D.该分子中的所有碳原子不可能共平面 |
结构为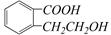 的有机物可以通过不同的反应得到下列四种物质:
的有机物可以通过不同的反应得到下列四种物质:
①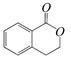 ②
② ③
③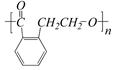 ④
④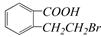 ,
,
生成这四种有机物的反应类型依次为:
| A.取代、消去、酯化、加成 | B.酯化、消去、缩聚、取代 |
| C.酯化、取代、缩聚、取代 | D.取代、消去、加聚、取代 |
苯环结构中不存在碳碳单键与碳碳双键的交替结构,可以作为证据的是
①苯不能使溴水褪色
②苯不能使酸性高锰酸钾溶液褪色
③苯在一定条件下既能发生取代反应,又能发生加成反应
④经测定,邻二甲苯只有一种结构
⑤经测定,苯环上碳碳键的键长相等,都是1.40×10-10m
| A.①②④⑤ | B.①②③⑤ | C.①②③ | D.①② |