已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,判断下列叙述中正确的是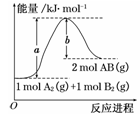
| A.每生成2分子AB吸收b kJ热量 |
| B.该反应热ΔH=+(a-b) kJ·mol-1 |
| C.该反应中反应物的总能量高于生成物的总能量 |
| D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量 |
某温度时,浓度都是1 mol·L-1的两种气体X2和Y2,在密闭容器中发生可逆反应生成气体Z,充分反应后X2的浓度为0.4 mol·L-1,Y2的浓度为0.8 mol·L-1,生成的Z的浓度为0.4 mol·L-1,则该反应的化学方程式(Z用X、Y表示)是( )
A.X2+2Y2 2XY2 2XY2 |
B.2X2+Y2 2X2Y 2X2Y |
C.X2+3Y2 2XY3 2XY3 |
D.3X2+Y2 2X3Y 2X3Y |
反应4A(s)+3B(g) 2C(g)+D(g),经2 min B的浓度减少0.6 mol·L-1。对此反应速率的正确表示是( )
2C(g)+D(g),经2 min B的浓度减少0.6 mol·L-1。对此反应速率的正确表示是( )
A.用A表示的反应速率是0.8 mol·L-1·s-1
B.分别用B、C、D表示反应的速率,其比值是3∶2∶1
C.在2 min末时的反应速率,用反应物B来表示是0.3 mol·L-1·min-1
D.在这2 min内用B和C表示的反应速率的值都是相同的
在一定条件,将A2和B2两种气体通入1 L密闭容器中,发生反应:xA2(g)+yB2(g) 2C(g)。2 s内的反应速率:v(A2)=0.5 mol·L-1·s-1,v(B2)=1.5 mol·L-1·s-1,v(C)="1" mol·L-1·s-1。则x和y的值分别为( )
2C(g)。2 s内的反应速率:v(A2)=0.5 mol·L-1·s-1,v(B2)=1.5 mol·L-1·s-1,v(C)="1" mol·L-1·s-1。则x和y的值分别为( )
A.2和3 B.3和2 C.3和1 D.1和3
某一反应物的浓度是2.0 mol·L-1,经过4 min后,它的浓度变成1.68 mol·L-1,则在这4 min内它的平均反应速率为( )
| A.0.2 mol·L-1·min-1 |
| B.0.1 mol·L-1·min-1 |
| C.0.04 mol·L-1·min-1 |
| D.0.08 mol·L-1·min-1 |
下列说法正确的是( )
| A.化学反应速率通常用单位时间内反应物或生成物的质量变化来表示 |
| B.用不同物质的浓度变化表示同一时间内、同一反应的速率时,其数值之比等于反应方程式中对应物质的化学计量数之比 |
| C.化学反应速率的单位由浓度单位决定 |
| D.在反应过程中,反应物的浓度逐渐变小,所以用反应物表示的化学反应速率为负值 |