元素周期律揭示元素间的递变规律,既有相似性又有递变性,下列递变规律正确的是
| A.第二周期元素氢化物稳定性的顺序是:HF>H2O,所以第三周期元素氢化物稳定性的顺序也是:HCl>H2S |
| B.IVA族元素氢化物熔点顺序是:SiH4>CH4,所以VA族元素氢化物熔点顺序也是:PH3>NH3 |
| C.ⅦA族元素的非金属性是:F>Cl,所以ⅦA族元素氢化物的酸性也是:HF>HCl |
| D.镁比铝活泼,工业上用电解熔融氧化铝制备铝,所以工业上也用电解熔融氧化镁制备镁 |
为检验试管中少量白色晶体是否为铵盐,下列四位同学分别设计了四种方案,其中最好的方案是
| A.加入1 mLNaOH溶液,将湿润的蓝色石蕊试纸靠近试管口 |
| B.加入1 mLNaOH溶液,将干燥的红色石蕊试纸靠近试管口 |
| C.加入1 mLNaOH溶液,加热试管,将干燥的蓝色石蕊试纸靠近试管口 |
| D.加入1 mLNaOH溶液,加热试管,将湿润的pH试纸靠近试管口 |
下列实验报告记录的实验现象正确的是
| 实验 |
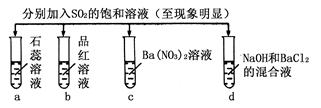 |
||||
| 记 录 |
a |
b |
c |
d |
|
| A |
无色 |
不褪色 |
无色溶液 |
无色溶液 |
|
| B |
红色 |
无色 |
白色沉淀 |
白色沉淀 |
|
| C |
红色 |
无色 |
无色溶液 |
白色沉淀 |
|
| D |
无色 |
无色 |
白色沉淀 |
无色溶液 |
以下说法正确的是
| A.白磷与金刚石一样,晶体中原子以共价键结合,形成空间网状结构 |
| B.CO2和SiO2晶体中,化学键类型相同,晶体类型也相同 |
| C.共价化合物可以含离子键 |
| D.NH4Cl晶体中既含有离子键又含有共价键 |
已知拆开1molH2中的化学键需要消耗436kJ能量,拆开1molO2中化学键需要消耗496kJ能量,形成水分子中1molH-O键释放463kJ能量,则下列热化学方程式正确的是
| A.2H2+O2=2H2O;⊿H=-484kJ•mol-1 |
| B.2H2(g)+O2(g)=2H2O(l);⊿H=-484kJ•mol-1 |
| C.2H2(g)+O2(g)=2H2O(g);⊿H=-484kJ•mol-1 |
| D.2H2(g)+O2(g)=2H2O(g);⊿H=+484kJ•mol-1 |
在2A(g)+ B(g)="3C(g)+" 4D(g)反应中,表示该反应速率最快的数据是
A.υ(A)= 0.6mol·L-1·s-1 B.υ(B)=" 0.2" mol·L-1·s-1
C.υ(C)=" 0.8" mol·L-1·s-1 D.υ(D)=" 1.0" mol·L-1·s-1