下列离子方程式书写正确的是
| A.FeCl2溶液中通入氯气:Fe2++Cl2═Fe3++2Cl﹣ |
| B.澄清石灰水与少量小苏打溶液混合:Ca2++OH﹣+HCO3﹣═CaCO3↓+H2O |
| C.FeS固体放入稀硝酸溶液中:FeS+2H+═Fe2++H2S↑ |
| D.碳酸氢镁和足量的氢氧化钙溶液反应:Ca2++OH﹣+HCO3﹣═CaCO3↓+H2O |
在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2的化合物是:( )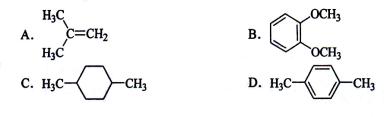
由2—氯丙烷为主要原料制取1,2—丙二醇CH3CH(OH)CH2OH时,经过的反应为( )
| A.加成—消去—取代 | B.消去—加成—取代 |
| C.取代—消去—加成 | D.取代—加成—消去 |
下列有机物的命名正确的一组是 ()
A.二溴乙烷 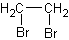 |
B.3-乙基-1-丁烯  |
C.2-甲基-2,4-己二烯 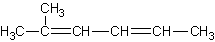 |
D.2-甲基-1-丙醇 |
下列说法中错误的是
| A.若XY4分子中X原子处于正四面体的中心,则XY4分子为非极性分子 |
| B.C2H5OH与C2H5Br相比,前者的相对分子质量远小于后者,而沸点却远高于后者,其原因是前者的分子间存在氢键 |
| C.CO2与SiO2晶体熔化时,所克服的微粒间相互作用相同 |
| D.短周期元素离子aXm+和bYn-具有相同的电子层结构,则a>b |
有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是
| A.若X(OH)n为强碱,则Y(OH)n也一定为强碱 |
| B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性 |
| C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2 |
| D.若Y的最高正价为+m,则X的最高正价一定为+m |