A~G各物质间的关系如图,其中B、D为气态单质。

请回答下列问题:
(1)物质C、E分别为 、 。(填名称)
(2)反应①可选用不同的A进行,若反应在常温下进行,其化学方程式为 。
(3)请设计实验检验F、G的混合溶液中F的金属阳离子。(写出试剂、操作、现象、结论) 。
图中X、Y、Z为单质,其他为化合物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应,回答下列问题: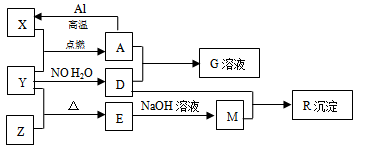
(1)M中存在的化学键类型为_______________________;
(2)一定条件下,Z与H2反应转化为ZH4,ZH4的电子式为_______________;
(3)已知A与1molAl反应转化为X时(所有物质均为固体)的热效应为akJ,则该反应的热化学方程式为_______________;
(4)A与过量D的稀溶液反应生成G的离子方程式为_______________;
(5)向含4molD的稀溶液中,逐渐加入X粉末至过量.假设生成的气体只有一种,请在坐标系图乙中画出n(X2+)随n(X)变化的示意图,并标出n(X2+)的最大值。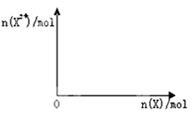
主族元素W、X、Y、Z的原子序数依次增大,W原子最外层电子数是次外层的3倍,X,Y和Z分属于不同的周期,它们的原子序数之和是W原子序数的5倍。在由元素W、X、Y、Z组成的所有二组分化合物中,由元素W、Y形成的化合物M的熔点最高。请回答下列问题:
(1)W原子L层电子排布式为 W3空间构形是
(2)X单质与水反应的主要化学方程式
(3)化合物M的化学式 其晶体结构与NaCl相同,而熔点高于NaCl。M熔点较高的原因是 。将一定是的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂酸醇酯交换合成碳酸二月桂酯。在碳酸二甲酯分子中,碳原子采用的杂化方式有 ,O-C-O的键角约
(4) X、Y、Z可形成立方晶体的化合物,其晶胞中X占有棱的中心,Y位于顶角,Z位于体心位置,则该晶体的组成为X:Y:Z= 。
(5)含有元素Z的盐的焰色反应为 色,许多金属盐都可以发生焰色反应,其原因是
(6) ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,其晶胞边长为540.0 pm,密度为 g·cm-3(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为____________pm。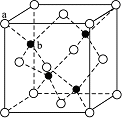
[化学选修5—有机化学基础]
药物菲那西洒汀的一种合成路线如下: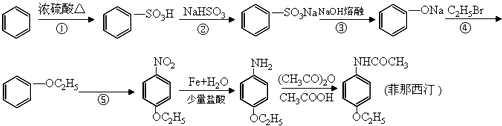
(1)菲那西汀的分子式 _____________________;
(2)①~⑥反应过程中在苯环上发生取代反应的是_____________________;
(3)反应②中生成的无机物的化学式为 _____________________;
(4)写出⑤反应的化学方程_____________________;
(5)菲那西汀水解的化学方程式是_____________________;
(6)菲那西汀的同分异构体中,符合下列条件的共有_______种;
①含苯环且只有对位两个取代基②苯环上含有氨基③能水解,水解产物能发生银镜反应
(7)菲那西汀的同分异构体中,含苯环且只有对位两个取代基,两个取代基含有相同碳原子数,且含有α-氨基酸结构,写出这种同分异构体缩聚后高分子产物的结构简式_____________________。
某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。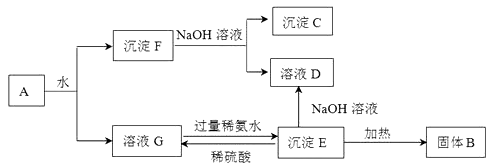
请回答下列问题。
(1) 图中涉及分离溶液与沉淀的方法是__________________。
(2) B、C、D、E 4种物质的化学式为:B_________、C_________、D_________、E_________。
(3)沉淀F与NaOH溶液反应的离子方程式为
沉淀E与稀硫酸反应的离子方程式为
溶液G与过量稀氨水反应的化学方程式为
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。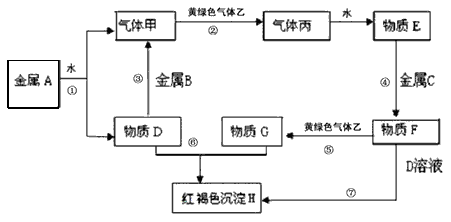
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A___________、B___________、C____________、
F___________、H___________、乙____________。
(2)写出下列反应离子方程式:
反应①______________________
反应⑥_____________________