四种基本反应类型与氧化还原反应的关系如下图所示,则下列化学反应中属于区域3的反应是
| A.Zn + H2SO4 = ZnSO4 + H2↑ |
B.H2 + Cl2 2HCl 2HCl |
C.2KClO3 2KCl+3O2↑ 2KCl+3O2↑ |
| D.2Cl2+2Ca (OH)2 = CaCl2+Ca(ClO)2+2H2O |
某物质的结构简式如图所示,关于该物质的说法正确的是()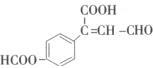
| A.1mol该物质最多能和3mol氢气发生加成反应 |
| B.1mol该物质和银氨溶液反应,最多可生成2mol银 |
| C.1mol该物质最多能和3mol氢氧化钠发生反应 |
| D.1mol该物质和碳酸钠反应可生成1mol二氧化碳 |
结构为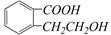 的有机物可以通过不同的反应得到下列四种物质:
的有机物可以通过不同的反应得到下列四种物质:
①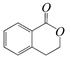 ②
②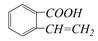 ③
③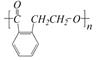 ④
④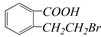 ,
,
生成这四种有机物的反应类型依次为()
| A.取代、消去、酯化、加成 | B.酯化、消去、缩聚、取代 |
| C.酯化、取代、缩聚、取代 | D.取代、消去、加聚、取代 |
以下烃中,一氯代物只有一种的是()
| A.丙烷 | B.正丁烷 | C.正戊烷 | D.新戊烷 |
化合物A(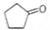 )可由环戊烷经三步反应合成:()
)可由环戊烷经三步反应合成:() ,则下列说法错误的是
,则下列说法错误的是
| A.反应1可用的试剂是氯气 |
| B.反应1为取代反应,反应2为消去反应 |
| C.反应3可用的试剂是氧气和铜 |
| D.1molA完全燃烧消耗6mol氧气 |
下列有机化合物命名正确的是()
A.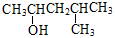 :4-甲基-2-戊醇 :4-甲基-2-戊醇 |
| B.HCOOCH2CH3:丙酸 |
C.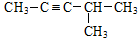 :2-甲基-3-戊炔 :2-甲基-3-戊炔 |
D. :2-甲基丁醛 :2-甲基丁醛 |