钠与水反应的现象与钠的下列性质无关的是
| A.钠的熔点较低 | B.钠的密度小于水 |
| C.钠的硬度较小 | D.钠很活泼 |
已知室温时,0.1 mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是 ( )
| A.该溶液的pH=4 |
| B.降低温度,溶液的pH减小 |
| C.此酸的电离平衡常数约为1×10-7 |
| D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
下列四种溶液:
①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;
④pH=12的NaOH溶液.相同条件下,有关上述溶液的比较中,正确的是( )
| A.将②、③两种溶液混合后,若pH=7,则消耗溶液的体积:②>③ |
| B.由水电离的c(H+):①=②>③=④ |
| C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大 |
| D.向等体积的四种溶液中分别加入100 mL水后,溶液的pH:③>④>①>② |
下列各溶液中微粒的物质的量浓度关系表述正确的是( )
A.0.1mol·L-1的 溶液中:c( 溶液中:c(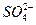 )>c( )>c(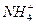 )> )>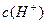 > >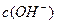 |
B.0.1mol·L-1的NaHCO3溶液中:c(Na+)=c(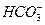 )+c( )+c( )+2c( )+2c(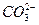 ) ) |
| C.将0.2mol·L-1 NaA溶液和0.1mol·L-1盐酸等体积混合所得碱性溶液中: c(Na+)+c(H+)=c(A-)+c(Cl-) |
|
D.在250C 100mL NH4Cl溶液中:c(Cl-)=c(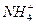 )+c(NH3·H2O) )+c(NH3·H2O) |
观察下列几个装置示意图,有关叙述正确的是( )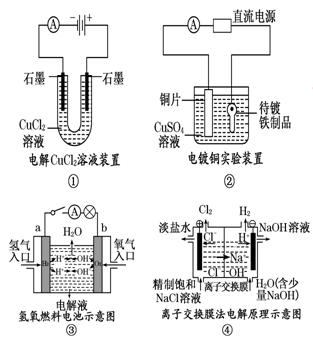
| A.装置①中阳极上析出红色固体 |
| B.装置②的待镀铁制品应与电源正极相连 |
| C.装置③中外电路电子由a极流向b极 |
| D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 |
化学平衡常数K的数值大小是衡量化学反应进行程度的标志,在同一条件下,下列反应的平衡常数的数值如下:
2NO(g) N2(g)+O2(g) K1=1×1030
N2(g)+O2(g) K1=1×1030
2H2(g)+O2(g)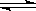 2H2O(g) K2=2×1081
2H2O(g) K2=2×1081
2CO2(g)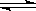 2CO(g)+O2(g) K3=4×10-92
2CO(g)+O2(g) K3=4×10-92
在同一条件下,以下说法正确的是( )
| A.NO分解产生O2的反应的平衡常数表达式为K1=c(N2)·c(O2) |
| B.水分解产生O2,此时平衡常数的数值约为5×10-80 |
| C.NO、H2O、CO2三种化合物分解放出O2的倾向由大到小的顺序为NO>H2O>CO2 |
| D.以上说法都不正确 |