下列说法正确的是
| A.强酸跟强碱的反应热一定是中和热 |
| B.1molC完全燃烧放热383.3kJ,其热化学方程为: C+O2=CO2ΔH=-383.3kJ·mol-1 |
| C.在稀溶液中,酸与碱发生中和反应生成1 mol H2O时的反应热叫做中和热 |
| D.表示中和热的离子方程式为: |
H+(aq)+OH-(aq) H2O(l);ΔH=57.3KJ·mol-1
H2O(l);ΔH=57.3KJ·mol-1
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为硫酸,工作时反应为:
Pb+PbO2+2H2SO4===2PbSO4+2H2O
下列结论正确的是( )
| A.Pb为正极被氧化 |
| B.SO42—只向PbO2极移动 |
| C.电解质溶液密度不断减小 |
| D.溶液的pH值不断减小 |
燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如图所示,a、b均为惰性电极。下列叙述不正确的是( )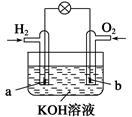
| A.a极是负极,该电极上发生氧化反应 |
| B.b极反应是O2+4OH--4e-===2H2O |
| C.总反应方程式为2H2+O2===2H2O |
| D.氢氧燃料电池是一种具有应用前景的绿色电源 |
日常所用干电池的电极分别为石墨棒(上面有铜帽)和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加入MnO2吸收H2),电极反应式可简化为:Zn-2e-===Zn2+,2NH+2e-===2NH3↑+H2↑(NH3与Zn2+能生成一种稳定的物质)。根据上述判断,下列结论正确的是( )
①锌为正极,石墨为负极 ②锌为负极,石墨为正极
③工作时,电子由石墨极经过外电路流向锌极
④长时间连续使用时,内装糊状物可能流出腐蚀用电器
| A.①③ | B.②③ | C.③④ | D.②④ |
下列有关电池的说法不正确的是( )
| A.手机上用的锂离子电池属于二次电池 |
| B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C.甲醇燃料电池可把化学能转化为电能 |
| D.锌锰干电池中,锌电极是负极 |
据报道,美国正在研究用锌电池取代目前广泛使用的铅蓄电池,锌电池具有容量大、污染少等优点,其电池反应为2Zn+O2===2ZnO,其原料为锌粉、电解液和空气。则下列叙述正确的是( )
| A.锌为正极,空气进入负极 |
| B.负极反应为Zn-2e-===Zn2+ |
| C.正极发生氧化反应 |
| D.电解液是酸溶液 |