在密闭容器中发生反应:aX(g)+bY(g)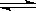 cZ(g)+dW(g),反应达到平衡后,保持温度不变,将气体体积压缩到原来的1/2,当再次达到平衡时,W的物质的量浓度为原平衡的1.8倍。下列叙述中不正确的是
cZ(g)+dW(g),反应达到平衡后,保持温度不变,将气体体积压缩到原来的1/2,当再次达到平衡时,W的物质的量浓度为原平衡的1.8倍。下列叙述中不正确的是
| A.平衡向逆反应方向移动 | B.a + b < c + d |
| C.Y的体积分数减小 | D.X的转化率下降 |
一定温度下,甲、乙两瓶氨水的浓度分别为1mol/L和0.1mol/L,则甲、乙两瓶氨水中c(OH—)
之比为
| A.大于10 | B.小于10 | C.等于10 | D.无法确定 |
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
| A.SO2和SiO2 | B.CCl4和KCl | C.NaCl和HCl | D.CO2和H2O |
中学化学中很多“规律”都有其使用范围,下列根据有关“规律”推出的结论合理的是
| A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 |
| B.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
| C.根据溶液的pH与溶液酸碱性的关系,推出pH=6.8的溶液一定显酸性 |
| D.根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |
下列中心原子采取sp2杂化且为非极性分子的是:
| A.CS2 | B.H2S | C.SO2 | D.SO3 |
下列表达式错误的是
A.碳-12原子表示为  |
B.氮原子的L层电子的电子排布图 |
| C.硫离子的核外电子排布式1s22s22p63s23p6 |
D.NH4Cl的电子式为: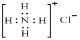 |