原水(未经处理的水)中含有泥沙悬浮物和细菌等杂质,可用次氯酸杀死细菌。氯气溶解于水时,可生成盐酸和次氯酸。某水厂生产自来水的净化步骤如下:

(1)可以除去大颗粒悬浮物杂质的步骤是____________。(填标号)。
(2)该厂生产的自来水是 _______________。(填纯净物或混合物)
(3)A步中加明矾的作用为__________________________。
(4)请你写出一点生活中节约用水的方法:___________________________
(5)饮用硬度过大的水不利于人体健康,可用 区分硬水和软水,在生活中可通过 方法来降低水的硬度.
(6)自制净水器中常加入 ,用于除去水中的异味和色素
(7)茶杯内的纱网,可将茶叶与茶水分离,便于饮用,该设计利用的化学原理是 。
某同学用固体氯化钾配制8
的氯化钾溶液,实验室现有①托盘天平;②量筒;③烧杯;④玻璃棒;⑤酒精灯等仪器.请按要求回答下列问题:
(1)配制100
质量分数为8
的氯化钾溶液,所需氯化钾的质量为
.
(2)用托盘天平称量所需的氯化钾.托盘天平调节平衡后,接下来的操作应该是(填字母).
A.先在左盘纸片上加氯化钾,后在右盘纸片上加砝码
B.先在右盘纸片上加砝码,后在左盘纸片上加氯化钾.
(3)配制溶液过程中,上述仪器不需要的是(填序号).
(4)该同学将配制好的溶液装入试剂瓶中,请你帮助他在如图所示的标签内写好标签的内容.
某研究性学习小组利用下列装置进行气体的制取,请分析并填空.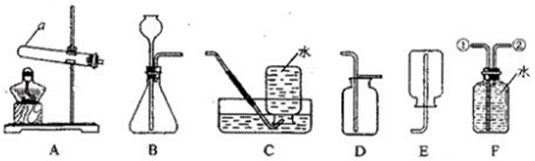
(1)写出图中仪器a的名称:。
(2)实验室用大理石和稀盐酸反应制取二氧化碳的化学方程式为,应选择制取并收集的装置为(填字母)。
⑶实验室用加热氯酸钾和二氧化锰混合物制取氧气,应选择发生装置为(填字母);若用盛满水的F装置收集氧气,氧气应从导管(填①或②)处通入F装置。
⑷若锌和镁混合物的质量为4.8g与100g稀硫酸恰好完全反应,则该稀硫酸的溶质质量分数可能是(填字母)。
| A. | 5% | B. | 10% | C. | 15% | D. | 20% |
联合国将
年定为"国际化学年",以彰显化学对知识进步、环境保护和经济发展做出的重要贡献.
(1)化肥的使用大幅度提高了粮食产量.如尿素
是一种常用的肥(填"氮"、"磷"、"钾").
(2)我国化学家侯德榜发明了联合制碱法,其反应原理的最后一步:加热碳酸氢钠生成纯碱,一种常用作溶剂的液体和一种能使澄清石灰水变浑浊的气体.写出该反应的化学方程式。
(3)科学家诺贝尔经过长期的试验,研制出安全炸药三硝酸甘油酯
.该炸药发生爆炸的化学方程式为:
,推断
的化学式为。
写出下列反应的化学方程式:
(1)硫在氧气中燃烧;
(2)锌片浸入硫酸铜溶液中;
(3)过氧化氢溶液中加入少量二氧化锰制取氧气。
根据原子结构的知识和下图的信息填空:
(1)甲图中①代表的元素符号是,乙图中所示元素原子的核电荷数是,丙图所示粒子属于(填"原子"、"阳离子"或"阴离子").
(2)写出甲、乙两种元素的单质间发生反应的化学方程式。