有关反应14CuSO4 +5FeS2 +12H2O =7Cu2S +5FeSO4 +12H2SO4,的下列说法错误的是
| A.FeS2既是氧化剂也是还原剂 |
| B.CuSO4在反应中被还原 |
| C.14 mol CuSO4氧化了1 mol FeS2 |
| D.被还原的S和被氧化的S的质量之比为3:7 |
常温下,下列离子浓度的关系正确的是
| A.0.2mol•L-1的CH3COONa溶液中c(CH3COO-)=a mol•L-1,0.1mol•L-1的CH3COONa溶液中c(CH3COO-)=b mol•L-1,则有a=2b |
| B.0.2mol•L-1的CH3COONa溶液与0.1mol•L-1的HCl溶液等体积混合,溶液显酸性:c(Na+)>c(Cl-)>c(CH3COO-)>c(H+)>c(OH-) |
| C.相同物质的量浓度的下列溶液中,c(NH4+)由大到小的顺序:(NH4)2SO4>(NH4)2CO3>NH4Cl>NH4HCO3 |
| D.0.1mol•L-1的HCN(弱酸)和0.1mol•L-1的NaCN等体积混合:c(HCN)+c(CN-)+c(OH-)=c(Na+)+c(H+) |
有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列各项的事实不能说明上述观点的是
| A.乙烷不能发生加成反应,而乙烯能发生加成反应 |
| B.苯在50℃~60℃时发生硝化反应,而甲苯在30℃时即可 |
| C.乙烷不能使酸性高锰酸钾溶液褪色,而甲苯能使酸性高锰酸钾溶液褪色 |
| D.乙醇不能与NaHCO3溶液反应,而乙酸能与NaHCO3溶液反应 |
对下列有机反应类型的认识中,错误的是
| A.苯乙烯使溴水褪色;加成反应 |
| B.乙烯水化生成乙醇;取代反应 |
| C.乙醇与CuO加热反应生成乙醛;氧化反应 |
| D.无水乙醇与浓硫酸加热到170℃制取乙烯;消去反应 |
天然橡胶是一种以聚异戊二烯为主要成分的天然高分子化合物,由异戊二烯人工合成的一种橡胶最接近天然橡胶,异戊二烯结构简式为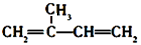 ,下列说法错误的是
,下列说法错误的是
| A.异戊二烯是乙烯的同系物 |
| B.异戊二烯分子中5个碳原子可能共平面 |
| C.异戊二烯与溴1:1加成可得3种产物(不考虑立体异构) |
| D.聚异戊二烯含有碳碳双键,能发生加成反应 |
下列有关实验叙述错误的是
| A.实验室可用硫酸铜溶液除去乙炔中的H2S等杂质气体 |
| B.苯和溴水在溴化铁溶液催化作用下发生取代反应生成溴苯 |
| C.只用溴水就可以将苯、四氯化碳、酒精、氢氧化钠溶液这四种物质区别开 |
| D.将铜丝在酒精灯上加热变黑后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |