下列观点正确的是
| A.化合物电离时,生成的阴离子是氢氧根离子的是碱 |
| B.某化合物的熔融状态能导电,该化合物中一定有离子键 |
| C.某化合物的水溶液能导电,该化合物一定是电解质 |
| D.某纯净物在常温下为气体,则组成该物质的微粒一定含有共价键 |
20℃时,将0.1 mol·L-1Na2S2O3溶液10 mL和0.01 mol·L-1 H2SO4溶液10 mL混合,
2 min后溶液中明显出现浑浊,已知温度每升高10℃,化学反应速率增大到原来的2倍,
那么50℃时,同样的反应要看到同样的浑浊,需要的时间是 ()
| A.40 s | B.15 s |
| C.48 s | D.20 s |
在一定温度时,N2与H2反应过程中能量变化的曲线如图。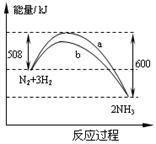
下列叙述正确的是()
A.该反应的热化学方程式为:N2+3H2 2NH3ΔH = -92 kJ/mol 2NH3ΔH = -92 kJ/mol |
| B.b曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的放热增多 |
| D.加入催化剂可增大正反应速率,降低逆反应速率 |
下列热化学方程式中△H代表燃烧热的是 ( )
| A.CH4(g)+3/2O2(g)=2H2O(g)+CO(g) △H1 |
| B.S(s)+3/2O2(g)=SO3(s)△H2 |
C.C6H12O6(s)+6O2(g)=6CO2( g)+6H2O(l) △H3 g)+6H2O(l) △H3 |
| D.2CO(g)+O2(g)=2CO2(g)△H4 |
已知在1×105Pa、298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )
| A.H2O(g)=H2(g)+1/2 O2(g); △H= +242kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l); △H= -484kJ·mol-1 |
| C.H2(g)+1/2 O2(g)=H2O(g); △H= +242kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(g); △H= -242kJ·mol-1 |
下列元素中属于人体生命活动必需微量元素的是
| A.H | B.O | C.Fe | D.Na |