下列离子方程式表示正确的是
| A.AgNO3溶液中加入Cu :Cu+Ag+=Cu2++Ag |
| B.NaHCO3溶液中加入CH3COOH: CO32-+2CH3COOH=CO2↑+2CH3COO-+H2O |
| C.含0.2mol FeBr2的溶液中通入0.2mol Cl2: 4Fe2++6Br-+5Cl2=4Fe3++3Br2+10Cl- |
| D.等体积等物质的量浓度的NaHCO3和Ba(OH)2溶液混合: |
HCO3-+Ba2++OH-=BaCO3↓+H2O
一定条件下,体积为2L的密闭容器中,1mol A和1mo1 B进行反应:A(g)+3B(g) 2C(g)经2分钟反应达到平衡,此时生成0.2mol C。
2C(g)经2分钟反应达到平衡,此时生成0.2mol C。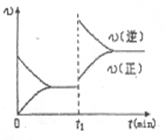
下列说法正确的是
A.反应开始至2分钟时,以B浓度变化表示的反应速率为0.05mol/(L.min)
B.反应开始至2分钟时,A的转化率为5%
C.若其他条件不变,升高温度,A的体积分数增大,则该反应的△H<0
D.若其他条件不变,增大压强,化学反应速率的变化符合右侧示意图
美国罗氏生产 的奥司他韦磷酸盐胶囊剂(商品名中国大陆称达菲·港译特敏福,台湾译为克流感)是市场上唯一的奥司他韦制剂。2009的,由于甲型H1N1在世界范围的扩散,全球掀起一般抢购达菲的风潮。奥司他韦的结构如图;下列说法正确的是
的奥司他韦磷酸盐胶囊剂(商品名中国大陆称达菲·港译特敏福,台湾译为克流感)是市场上唯一的奥司他韦制剂。2009的,由于甲型H1N1在世界范围的扩散,全球掀起一般抢购达菲的风潮。奥司他韦的结构如图;下列说法正确的是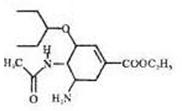
| A.奥司他韦是一种芳香族化合物,分子式为C18H28O4N3 |
| B.1mol该化合物可以和3mol氢气发生加成反应 |
| C.该化合物能发生水解反应,加成反应、氧化反应和消去反应 |
| D.奥司他韦可以和磷酸在一定条件下制取奥司他韦磷酸盐是由于具有碱性基团氨基 |
设NA代表阿伏加德罗常数的值,下列有关叙述正确的是
| A.0.1 mol Fe与足量的氯气反应时失去的电子数为0.2 NA |
| B.标准状况下22.4L SO3含有的分子数为NA |
| C.6gSiO2晶体中含有的硅氧键数目为0.4NA |
| D.用Pt做电极电解硫酸铜溶液,当阳极产生的气体在标准状况下为22.4L时,转移电子数目为2NA |
室温下,下列叙述正确的是(溶液体积变化忽略不计)
| ① |
② |
③ |
④ |
|||||
| 溶液 |
氨水 |
氢氧化钠溶液 |
醋酸 |
盐酸 |
||||
| pH |
11 |
11 |
3 |
3
|
下列离子方程式书写正确的是
| A.Fe3O4溶于稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| B.铝片溶于NaOH溶液:Al+2OH-=AlO2-+H2↑ |
| C.向苯酚钠溶液中通入少量CO2;C6H5O-+CO2+H2O→C6H5OH+HCO3- |
| D.向含1mol碘化亚铁的溶液中通入标准状况下22.4L氯气: |
2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-