二氧化钛是钛的重要化合物,钛白(纯净的二氧化钛)是一种折射率高、着色力和遮盖力强、化学性质稳定的白色颜料。从钛铁矿(主要成分FeTiO3,含Fe2O3、SiO2等杂质)制取二氧化钛,常用硫酸法,其流程如下:

(1)钛铁矿主要成分与浓硫酸反应的主要产物是TiOSO4和FeSO4,该反应的化学方程式 。
(2)为提高“固体熔块”水浸取时的浸出率,除了采用循环浸取、延长时间、熔块粉碎外,适宜的条件还可以选择 (任写一种)。
(3)过滤时所需玻璃仪器为漏斗、玻璃棒和烧杯。从滤液中得到X为绿矾(FeSO4·7H2O)晶体的实验操作依次为:加热浓缩、冷却结晶、过滤洗涤、低温干燥。实验室要配制、保存该溶液时需加少量铁屑,目的是 。
(4)第③步反应化学方程式 。
(5)若实验时需要450mL2mol/L的C溶液,则在精确配制时,需用托盘天平称取NaOH固体 g,所使用的仪器除托盘天平、量筒、烧杯、玻璃棒、胶头滴管、药匙外,还必须有 (填仪器名称)。
甲、乙两同学欲制取纯净的Fe(OH)2 ,根据如图所示的装置进行试验。A管中是Fe+H2SO4, B管中是NaOH溶液,请回答下列问题。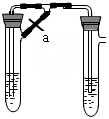
A B
(1)同学甲:先夹紧止水夹a,使A管开始反应,在B管中观察到的现象是 。
(2)同学乙:打开a,使A管中反应一段时间再夹紧止水夹a,实验中在B管中观察到的现象是 ,
B中发生反应的离子方程式为
(3)同学乙打开a的目的 , (填甲或乙)同学可成功。
红砖是用粘土高温烧结而成,因其颜色呈红色或棕红色而得名,常用作建筑材料。
(1)根据红砖的颜色、猜测其可能含有的成份是(写化学式)
(2)为了检验你的猜测是否正确,请设计一个实验方案,简要地写出各步操作过程以及最后的实验分析和结论,涉及化学反应的写出化学方程式(实验用品任取,该实验分几步自己决定,不必写实验装置中的仪器安装)
实验步骤:①用铁锤敲碎红砖,取小块磨成粉末。
②
③
④
实验分析及结论:
(3)红砖曾对我国建设起到重要作用,就目前我国实际情况看,你是认为应继续使用或者是禁止使用红砖?,理由是
( 6分)请你设计两种方法除去细小的铁颗粒中混有的细小的铝颗粒。(简要说明)
(1)
(2)
(10分)已知可逆反应CO + H2O(g) CO2 + H2,达到平衡时,
CO2 + H2,达到平衡时,
(1)830K时,若起始时:c (CO) =" 2" mol/L,c (H2O) =" 3" mol/L,平衡时CO的转化率为60%,水蒸气的平衡转化率为;K值为。
(2)830K,若只将起始时c (H2O)改为6 mol/L,则水蒸气的平衡转化率为。
(3)若830K时,起始浓度c (CO) =" a" mol/L,c (H2O) =" b" mol/L,H2的平衡浓度c (H2) =" c" mol/L,
①a、b、c之间的关系式是②当a = b时,a = c。
(10分)某研究性学习小组用电解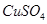 溶液的方法测定铜的相对原子质量(装置如图),实验中测得某电极的质量增重为m g,已知氧元素相对原子质量为16。请回答:
溶液的方法测定铜的相对原子质量(装置如图),实验中测得某电极的质量增重为m g,已知氧元素相对原子质量为16。请回答: 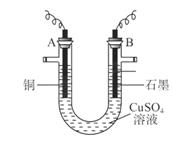
(1)m g应为极的质量增重(填A或B),电解总反应的离子方程式为;
(2)本实验(电解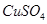 溶液)中,学习小组采用两套方案测定铜的相对原子质量。
溶液)中,学习小组采用两套方案测定铜的相对原子质量。
①第一套方案中,同学们测得气体的体积为V L(标准状况),则铜的相对原子质量是(用m、V表示);
②第二套方案中,以下数据需要测定的是(填序号)。
a. A极增加的质量 b. 整套装置减少的质量
c. 电解后溶液的体积 d. 电解后溶液的pH(可由此计算出溶液中H+的物质的量浓度)