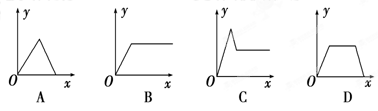氮化铝(AlN)是一种具有耐高温、抗冲击、导热性好等优良性质的物质,被广泛应用于电子工业、陶瓷工业。在一定条件下,氮化铝可通过如下反应合成
Al2O3 + N2 + 3C  2AlN + 3CO
2AlN + 3CO
下列叙述正确的是
| A.在该反应中,N2是氧化剂,Al2O3是还原剂 |
| B.在该反应中,每当生成2molAlN,N2失去6mol电子 |
| C.氮化铝中氮元素的化合价为-3价 |
| D.碳元素化合价升高,所以CO是还原剂 |
化学与人类生活、社会可持续发展密切相关。下列说法正确的是
| A.大量使用农药和化肥,以提高农作物产量 |
| B.用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 |
| C.天然药物无任何毒副作用,可长期服用 |
D.为改 善食品的色、香、味并防止变质,可加入大量食品添加剂 善食品的色、香、味并防止变质,可加入大量食品添加剂 |
10mL某气态的烃,在60mLO2里充分燃烧,得到液态水和体积为45mL的混合气体,则该烃可能是()
| A.甲烷 | B.丁烯 | C.丙烷 | D.乙烷 |
下列说法不正确的是()
A.甲烷和氯气反应 生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 |
| B.用溴水即可鉴别苯、四氯化碳、乙醇、裂化汽油 |
C.煤中含有苯 和甲苯,可以用先干馏后分馏的方法把它们分离出来 和甲苯,可以用先干馏后分馏的方法把它们分离出来 |
| D.蔗糖、麦芽糖的分子式都是C12H22O11,二者都属于低聚糖 |
下列关于有机物的说法正确的是()
| A.苯、乙酸和油脂都可以发生取代反应 |
| B.石油经过分馏得到的汽油、煤油等馏分都是纯净物 |
| C.乙烯、聚乙烯都能使酸性高锰酸钾溶液褪色 |
| D.在一定条件下,葡萄糖、淀粉、蛋白质都可发生水解反应 |
在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液直至过量。下列表示氢氧化钠加入量(x)与溶液中沉淀物的量(y)的关系示意图中,正确的是( )