某溶液中只含下表离子中的几种(不考虑水的电离与离子水解),且各离子的物质的量浓度均为0.1mol/L。
| 阳离子 |
K+ NH4+ Fe2+ Mg2+ Al3+ Cu2+ |
| 阴离子 |
OH- Cl- Al02- CO32- SiO32- SO42- |
某同学进行了如下实验(必要时可加热)

下列说法正确的是
A.原溶液中只含有NH4+ Fe2+ Cl- SO42-
B.由沉淀A推断原溶液中一定含有SO42-
C.滤液A中可能含有K+ Al3+ Cl-
D.沉淀B中一定含有Mg(OH)2
已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH  CH3COO-+H+,要使溶液中
CH3COO-+H+,要使溶液中 值增大,可以采取的措施是()
值增大,可以采取的措施是()
| A.加少量烧碱溶液 | B.降低温度 | C.加少量冰醋酸 | D.加水 |
可以将反应Zn+Br2 = ZnBr2设计成蓄电池,下列4个电极反应①Br2 + 2e-= 2Br-
②2Br- - 2e-= Br2 ③Zn – 2e-= Zn2+ ④Zn2+ + 2e-= Zn其中表示充电时的阳极反应和放电时的负极反应的分别是()
| A.②和③ | B.②和① | C.③和① | D.④和① |
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以A1作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l)
电解池:2Al+3H2O Al2O3+3H2↑电解过程中,以下判断正确的是()
Al2O3+3H2↑电解过程中,以下判断正确的是()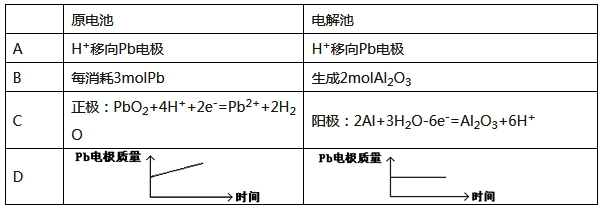
下列水解化学方程式或水解离子方程式正确的是()
A.CH3COO-+ H2O CH3COOH + OH- CH3COOH + OH- |
B.NH4+ + H2O NH4OH + H+ NH4OH + H+ |
C.CH3COOH + NaOH CH3COONa + H2O CH3COONa + H2O |
D.NaCl + H2O NaOH + HCl NaOH + HCl |
在水电离出的c(H+)=1×10-12 mol/L条件下,下列各组离子一定不能大量共存的是 ()
| A.NH4+、NO3-、Cl-、Na+ | B.K+、SO32-、Cl-、NO3- |
| C.Na+、SO42-、Cl-、HCO3- | D.Na+、NO3-、Fe3+、SO42- |