(16分) Ⅰ请回答:
(1)CO2的电子式____________________
(2)钠燃烧不能用CO2灭火,用化学方程式表示其理由________________
(3)重晶石(BaSO4)不溶于酸,用饱和Na2CO3处理转化为易溶于酸的BaCO3,写出反应的离子方程式__________________
Ⅱ。化合物K3Fe(A2B4)3.3H2O 是重要的催化剂。将化合物K3Fe(A2B4)3.3H2O受热完全分解,只得到气体产物和固体产物。 经分析,气体产物只有甲、乙和水蒸气。已知甲、乙均由A、B两元素组成,且摩尔质量:M(甲)>M(乙)。A元素的最外层电子数是次外层电子数的2倍,B元素的主族序数是其所在周期数的3倍。 经分析,固体产物只有Fe、FeO和K2AB3。某同学再进行以下定量分析。
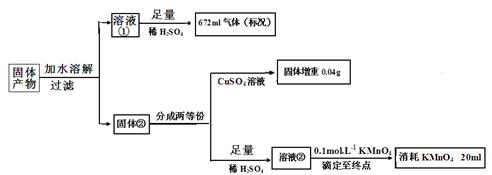
(1)甲的化学式:____________________
(2)溶液②与KMnO4发生氧化还原反应的离子方程式:_______________________
(3)由以上实验数据的分析可知n(Fe):n(FeO):n(K2AB3)= : :
(4)某同学认为:溶液②由紫红色变为无色,振荡试样半分钟内不变色,即可证明溶液②与KMnO4溶液反应达滴定终点。判断该同学设想的合理性并说明理由
截止到1999年,人们已经发现了113种元素,是否可以说我们已经发现了113种原子?为什么?
用原子序数为1~18的元素的元素符号及其形成的化合物的化学式填空
(1)原子半径最小的元素是
(2)最高价氧化物对应的水化物碱性最强的是
(3)最稳定的气态氢化物是
元素周期表的第三周期元素,从左到右,原子半径逐渐;元素的金属性逐渐,非金属性逐渐。该周期元素中,除稀有气体外,原子半径最大的是。
比较下列碱的碱性强弱: NaOHKOH 比较下列酸的酸性强弱: H2SO4HClO4比较下列气态氢化物的稳定性:H2ONH3
碱金属元素原子最外层的电子数都是个,碱金属元素中金属性最强的是,原子半径最小的是。卤素原子最外层的电子数都是个,;在卤族元素中非金属性最强的是。