下列说法正确的是
| A.准确量取24.00 mL的液体可选用量筒或滴定管 |
| B.配制0.1000mol·L-1碳酸钠溶液时,将溶液转移到容量瓶中需用玻璃棒引流 |
| C.用广泛pH试纸测得某溶液pH为3.5 |
| D.高锰酸钾是一种常用的化学试剂,当高锰酸钾晶体结块时,应在研钵中用力研磨,以得到细小晶体,有利于加快反应或溶解的速率 |
有关甲醛(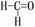 )、苯、二氧化碳及水说法不正确的是
)、苯、二氧化碳及水说法不正确的是
| A.苯与B3N3H6互为等电子体,且分子中原子共平面 |
| B.甲醛、苯和二氧化碳中碳原子均采用sp2杂化 |
| C.苯、二氧化碳是非极性分子,水和甲醛是极性分子 |
| D.水的沸点比甲醛高得多,是因为水分子间能形成氢键,而甲醛分子间不能形成氢键 |
近年来,科学家合成了一系列具有独特化学特性的(AlH3)n氢铝化合物。已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如图。下列有关说法肯定错误的是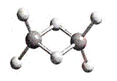
| A.化合物Al2H6中存在分子间作用力 |
| B.氢铝化合物可能成为未来的储氢材料和火箭燃料 |
| C.Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| D.Al2H6中含有离子键和极性共价键 |
A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子数之和;C元素是第3周期第一电离能最小的元素;D元素在第3周期中第一电离能最大。下列有关叙述错误的是
A.四种元素A、B、C、D分别为O、Ca、Na、Ar
B.元素A、B、C两两组成的化合物可为CaO、CaO2、Na2O、Na2O2等
C.元素A、C简单离子的半径大小关系为A<C
D.元素B、C电负性大小关系为B>C
下列叙述正确的是
①两种原子构成的共价化合物分子中的化学键都是极性键;
②两种不同非金属元素原子间形成的化学键都是极性键;
③含有非极性键的化合物一定是共价化合物;
④只要是离子化合物,其熔点就比共价化合物的熔点高;
⑤难失去电子的原子,易形成阴离子;
⑥单质分子中不存在化学键,化合物的分子中才存在化学键;
⑦离子化合物中一定含有离子键。
| A.只有②⑦ | B.只有①⑦ | C.只有⑦ | D.只有①⑤⑦ |
下列说法中正确的是
| A.非金属元素呈现的最高化合价不超过该元素原子的最外层电子数 |
| B.非金属元素呈现的最低化合价,其绝对值等于该元素原子的最外层电子数 |
| C.最外层有2个电子的原子都是金属原子 |
| D.最外层有5个电子的原子都是非金属原子 |