在500℃时,将足量的A固体投入2.0L真空密闭容器中,发生A(s) 2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示:
2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示:

(1)已知该反应只有高温下能自发进行,则该反应的△H 0(填“>”、“<”或“=”)。
(2)在上述反应条件下,从反应开始到平衡,用V(B)= mol·L-1·min-1,500℃时的平衡常数K= ;
(3)在反应温度和容器体积不变的条件下,下列能说明上述反应达到平衡状态的是 ;
A.混合气体的压强保持不变 B.气体C的体积分数保持不变
C.混合气体的密度保持不变 D.B的正反应速率等于C的逆反应速率
(4)在500℃时,上述反应达到平衡后,在8min时将容器体积迅速压缩为1.0L,反应在12min建立新的平衡,画出8~15min内C气体物质的量浓度随时间变化的示意图。
如下图所示,将铁、铜通过导线相连,置于稀硫酸中。
(1)铁片上的现象是,电极反应式。
(2)铜片上的现象是,电极反应式。
(3)写出该电池总反应的离子方程式。
在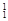 H,
H,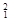 H,
H,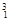 H,
H,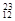 Mg,
Mg,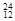 Mg,
Mg,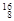 O,
O,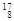 O,
O,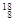 O中共有______种元素,______种原子,中子数最多的是。D218O的相对分子质量是______。
O中共有______种元素,______种原子,中子数最多的是。D218O的相对分子质量是______。
某温度时,在容积为2L的密闭容器中,三种气体物质的量随时间的变化曲线如图所示。请根据图中数据作答。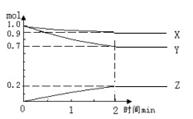
①列式计算在2分钟内X的化学反应速率
②写出该反应的化学方程式
③达到平衡时,Y的转化率为
下表是周期表中的一部分题目要求回答
| 族 周期 |
I A |
Ⅱ A |
Ⅲ A |
Ⅳ A |
Ⅴ A |
Ⅵ A |
Ⅶ A |
| 1 |
A |
||||||
| 2 |
E |
F |
|||||
| 3 |
B |
C |
D |
G |
H |
I |
(1)写出A元素的名称,H元素的符号
在这9种元素中,原子半径最大的是,画出G元素的原子结构示意图
A和F组成化合物的结构式元素F的单质电子式为
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是,呈两性的氢氧化物是。(填化学式)
(3)写出B的单质与水反应的化学方程式
(4)元素E的单质与Fe和稀硫酸构成原电池,试在右面的方框内画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出负极的电极反应为____________________。
 (5)在一定条件下,元素F与H2反应有一定限度(可理解为反应进行的程度),请判断在相同条件下元素G与H2反应的限度(选填“更大”、“更小”或“相同”)
(5)在一定条件下,元素F与H2反应有一定限度(可理解为反应进行的程度),请判断在相同条件下元素G与H2反应的限度(选填“更大”、“更小”或“相同”)
有以下各组微粒或物质:
| A.氯水和氯气; | B.35Cl和37Cl; | C.冰和干冰; | D.金刚石、石墨和C60 |
E、CO和CO2; F、氘和氚; G、O2和 O3; H、正丁烷和异丁烷;
其中,(1)互为同分异构体的有(填编号,以下同);
(2)互为同素异形体的有;
(3)互为同位素的有。