设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.在0.1 mol NaHSO4晶体中阳离子与阴离子总数为0.3NA |
| B.25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA |
| C.1.8 g D2O中含有的质子数和电子数均为NA |
| D.0.1molNa完全被氧化生成Na2O2时,转移的电子数目为0.1NA |
在盐类的水解过程中,下列各种情况必定发生的是
| A.盐的电离平衡被破坏 | B.水的电离平衡被破坏 |
| C.25℃,溶液的pH不是7 | D.溶液温度升高 |
已知;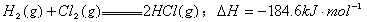 ,
,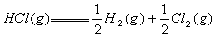
则反应的△H为
A.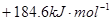 |
B.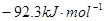 |
C.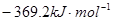 |
D.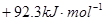 |
某学生用碱式滴定管量取0.1mol. L-1的NaOH溶液,开始时仰视液面,读数为11.00m L,取出部分溶液后俯视液面,读数为19.00m L,实际取出的体积为
| A.大于8.00m L | B.小于8.00m L | C.等于8.00m L | D.无法确定 |
水的电离过程为H2O H++OH-,在不同温度下其平衡常数为Kw(25℃)=1.0×10-14,Kw(35℃)=2.1×10-14。则下列叙述正确的是
H++OH-,在不同温度下其平衡常数为Kw(25℃)=1.0×10-14,Kw(35℃)=2.1×10-14。则下列叙述正确的是
| A.c(H+)随着温度升高而降低 | B.在35℃时,c(H+)>c(OH-) |
| C.蒸馏水中通HCl,Kw增大 | D.水的电离是吸热的 |
下列物质的稀溶液中存在电离平衡的有(不考虑水的电离)
| A.HBr | B.NaHSO4 | C.NH4NO3 | D.NaHCO3 |