常温下,将Cl2缓缓通入水中至饱和,然后向所得饱和溶液中滴加0.1mol·L-1NaOH溶液,整个过程中pH的变化如图所示。下列有关叙述正确的是
| A.从反应开始至②点,发生反应的离子方程式为:Cl2 +H2O ="=" ClO-+ 2H++ Cl- |
| B.③处表示氯气和NaOH溶液恰好完全反应 |
| C.②点所表示的溶液中所存在的具有氧化性的含氯元素的微粒主要有:Cl2、HClO、ClO- |
| D.从反应开始至②点可用pH试纸测定溶液的pH |
已知:CH4(g)+2O2(g)==CO2(g)+2H2O(1)△H = ―Q1 KJ/mol
2H2(g)+O2(g)==2H2O(g)△H = ―Q2 KJ/mol
2H2(g)+O2(g)==2H2O(1)△H = ―Q3KJ/mol
常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则放出的热量为多少KJ
| A.0.4Q1+0.05Q3 | B.0.4Q1+0.05Q2 |
| C.0.4Q1+0.1Q3 | D.0.4Q1+0.1Q2 |
2N2O5(g)=4NO2(g)+O2(g)△H=+56.8kJ/mol自发进行的原因是:( )
| A.是吸热反应; |
| B.是放热反应; |
| C.是熵减少的反应; |
| D.熵增大效应大于能量效应。 |
在一个固定体积的密闭容器中,加入2 mol A和1 mol B发生反应:2A(g)+B(g)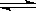 3C(g)+D(g),达到平衡时C的浓度为W mol·L-1。若维持容器体积和温度不变,按下列四种方法改变起始物质及其量,达到平衡后C的浓度仍为W mol·L-1的是( )
3C(g)+D(g),达到平衡时C的浓度为W mol·L-1。若维持容器体积和温度不变,按下列四种方法改变起始物质及其量,达到平衡后C的浓度仍为W mol·L-1的是( )
| A.4 mol A+2 mol B | B.2 mol A+1 mol B+3 mol C+1 mol D |
| C.3 mol C+1 mol D | D.3 mol C+1 mol D+1 mol B |
可逆反应mA(g) nB(g)+pC(s) ΔH=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是( )
nB(g)+pC(s) ΔH=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是( )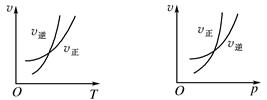
| A.m>n,Q>0 | B.m>n,Q<0 |
| C.m>n+p,Q>0 | D.m<n+p,Q<0 |
在一定温度下将1 mol CO和1 mol水蒸气放入一固定容积的密闭容器中,反应CO(g)+H2O CO2(g)+H2(g)达平衡后,得到0.6 mol CO2;再通入0.3 mol水蒸气,达到新平衡状态后,CO2的物质的量可能是( )
CO2(g)+H2(g)达平衡后,得到0.6 mol CO2;再通入0.3 mol水蒸气,达到新平衡状态后,CO2的物质的量可能是( )
| A.0.9 mol | B.0.7 mol | C.0.8 mol | D.0.6 mol |