在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入 a mol及b mol碘化氢(a>b),待反应2HI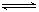 I2 (g)+H2(g) 达平衡后,下列说法肯定正确的是
I2 (g)+H2(g) 达平衡后,下列说法肯定正确的是
A.从反应开始到建立平衡所需时间:tA<tB
B.平衡时I2的浓度:c(I2)A = c(I2)B
C.平衡时碘蒸气在混合气体中的百分含量:A容器大于B容器
D.平衡时HI的分解率:αA= αB
下列说法正确的是
| A.标准状况下,6.02×1023个分子所占的体积约是22.4L |
| B.0.5mol氢气所占的体积约为11.2L |
| C.标准状况下,1mol H2O的体积为22.4L |
| D.25℃,1.01×105 Pa,32克O2和O3的混合气体所含原子数为2NA |
已知自然界氧的同位素有16O , 17O ,18O,若氢的同位素有H、D、T,从水分子的原子组成来看,自然界的水一共有几种
A.18种 B.6种 C.9种D.12种
在相同温度和压强下,下列气体密度最小的是
| A.CO2 | B.H2 | C.O2 | D.Cl2 |
不同固态物质分子1 mol,体积大小并不相同,主要原因是
| A.微粒大小不同 | B.微粒质量不同 |
| C.微粒间平均距离不同 | D.微粒间引力不同 |
下列实验操作中错误的是
| A.蒸发结晶操作时,当有大量晶体析出时停止加热,用余热蒸干 |
| B.蒸馏操作时,应使温度计水银球插入液态混合物中 |
| C.分液操作时,分液漏斗中下层液体从下口流出,上层液体从上口倒出 |
| D.萃取操作时,萃取剂要和原溶剂互不相溶,且不能与溶质和溶剂反应 |