H2S废气资源化利用途径之一是回收能量并得到单质硫。反应原理为:2H2S(g) + O2(g) = S2(s) + 2H2O(l) △H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法正确的是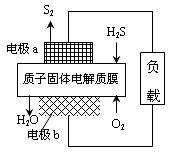
| A.电极a为电池的正极 |
B.电极b上发生的电极反应为:O2+2H2O+4e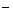 =" 4" OH =" 4" OH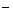 |
| C.电路中每流过4mol电子,电池内部释放632kJ热能 |
| D.每17gH2S参与反应,有1mol H+经质子膜进入正极区 |
在四个不同的容器中,在不同条件下进行反应:N2+3H2 2NH3根据在相同时间内测定的结果判断,生成氨气的速率最快的是
2NH3根据在相同时间内测定的结果判断,生成氨气的速率最快的是
| A.υ(H2)=0.2mol·L-1·s-1 | B.υ(N2)=0.4mol·L-1·min-1 |
| C.υ(NH3)=0.3mol·L-1·s-1 | D.υ(H2)=0.6mol·L-1·min-1 |
下列离子方程式书写正确的是
| A.醋酸与氨水反应:CH3COOH+NH3•H2O═CH3COO-+NH4+ + H2O |
| B.氯气跟水反应:Cl2+H2O=2H++Cl-+ClO- |
| C.钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
| D.硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
下列关于浓硫酸的说法中,不正确的是
| A.常作为气体的干燥剂 | B.滴在蔗糖上,蔗糖会变黑 |
| C.常温下不能与铁发生反应 | D.工业上主要采用接触法制备 |
分析下图的能量变化示意图,下列选项正确的是
| A.2C====2A+B;ΔH>0 |
| B.2A+B====2C;ΔH>0 |
| C.2C(g)="===" 2A(g)+B(g);ΔH<0 |
| D.2A(g)+B(g)====2C(g);ΔH<0 |
下列物质的水溶液中,呈碱性的是
| A.Na2CO3 | B.Na2SO4 | C.NH4Cl | D.KAl (SO4) 2 |