设阿伏加德罗常数为NA,下列说法正确的是
| A.22.4 LCl2分别与铁和铜反应时,失电子数目均为NA |
| B.1mol Na2O2与CO2足量反应时,转移NA个电子 |
| C.1mol·L-1的NaOH溶液中含Na+数目为NA |
| D.1mol Na2O2晶体中含有的阴离子数目为2NA |
25℃时,某溶液中由水电离产生的C(H+)和C(OH-)的乘积为1×10-20,下列说法正确的是
| A.该溶液的pH一定是10 | B.该溶液不可能pH="4" |
| C.该溶液的pH不可能是7 | D.不会有这样的溶 |
下列说法正确的是
| A.pH=2和pH=1的硝酸中c(H+)之比为1:10 |
B.Na2CO3溶液c(Na+)与c(CO )之比为2:1 )之比为2:1 |
| C.0.2 mol/L与0.1 mol/L醋酸中c(H+)之比为2:1 |
| D.pH=1的硫酸中加入等体积0.05 mol/L的BaCl2溶液,两者恰好反应C(SO42-)=0 |
“84”消毒夜在日常生活中被广泛使用。该消毒液无色,pH大于7,对某些有色物质有漂白作用。你认为它可能的有效成分是
| A.SO2 | B.Na2CO3 | C.KMnO4 | D.NaClO |
如图所示实验,如x轴表示流入阴极的电子的物质的量,则y轴可表示
①c(Ag+) ②c(NO3-) ③a棒的质量 ④b棒的质量 ⑤溶液的pH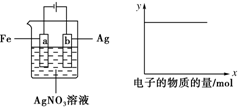
| A.①③ | B.③④ | C.①②④ | D.①②⑤ |
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图。下列说法正确的是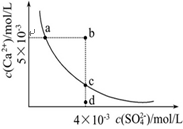
常温下,向100mL CaSO4饱和溶液中,加入400mL 0.01mol/LNa2SO4溶液后,溶液中有沉淀析出
B.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×10-3 mol/L
C.d点溶液通过蒸发可以变到c点
D.a点对应的Ksp等于c点对应的Ksp