在一密闭容器中有如下反应:L (s) + a G (g)  b R (g) 温度和压强对该反应的影响如图所示,其中压强P1 < P2,由此可判断
b R (g) 温度和压强对该反应的影响如图所示,其中压强P1 < P2,由此可判断
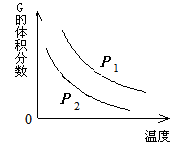
| A.正反应为放热反应 |
| B.化学方程式中的计量数a > b |
| C.G的转化率随温度升高而减小 |
| D.增大压强,容器内气体质量不变 |
下列化合物,既能发生消去反应,又能发生催化氧化反应的是
| A.CH3OH | B.C2H5OH |
C.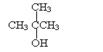 |
D.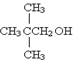 |
下列分子式表示的物质一定是纯净物的是
| A.C2H6O | B.C2H4Cl2 | C.CH4O | D.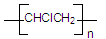 |
除去括号内杂质所用试剂和方法,正确的是
| 选项 |
物质 |
所用试剂 |
方法 |
| A. |
乙醇(乙酸) |
碳酸钠溶液 |
分液 |
| B. |
溴苯(溴) |
氢氧化钠溶液 |
蒸馏 |
| C. |
乙酸乙酯(乙酸) |
饱和碳酸钠溶液 |
过滤 |
| D. |
乙醇(水) |
生石灰 |
蒸馏 |
有八种物质:①甲烷 ②苯 ③聚乙烯 ④乙烯 ⑤2-丁炔 ⑥环己烷 ⑦邻二甲苯 ⑧环己烯,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是
| A.③⑤⑧ | B.④⑤⑦ | C.④⑤⑧ | D.⑤⑦⑧ |
与CH2=CH2 ® CH2Br—CH2Br的变化属于同一反应类型的是
| A.CH3CHO®C2H5OH |
| B.C2H5OH®CH2=CH2 |
C. |
| D.CH3COOH®CH3COOC2H5 |