设NA表示阿伏加德罗常数,下列说法正确的是
| A.1molHCl中含有NA个质子 |
| B.0.1mol冰醋酸、0.1mol无水乙醇和浓硫酸混合加热后可得0.1NA个乙酸乙酯分子 |
| C.标准状况下,11.2 L乙醇中所含的碳原子数目为NA |
| D.16g的O2与O3混合物中氧原子数为NA |
下列说法正确的是()
| A.某溶液滴入AgNO3溶液,产生白色沉淀,则这种溶液中一定含有氯离子 |
| B.某溶液与淀粉KI溶液混合后,出现蓝色,则证明该溶液是氯水或溴水 |
| C.氟气与NaCl水溶液反应后,一定有HF和O2生成 |
| D.氯水能使所有有色物质褪色 |
向含有NaBr、KI的溶液中通入过量的Cl2,然后将溶液蒸干,并灼烧固体,最后得到的物质是()
| A.KCl | B.NaCl和KCl | C.NaCl和KBr | D.NaCl、KCl和I2 |
除去氯气中混有的少量的氯化氢,最好选用( )
| A.水 | B.饱和食盐水 | C.纯碱溶液 | D.烧碱溶液 |
| A.b+n+m | B.b+n-m |
| C.b-n-m | D.b-n+m |
A.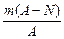 mol mol |
B.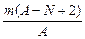 mol mol |
C. mol mol |
D.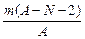 mol mol |