下图是某同学配制50克质量分数为5%的盐水的全过程

(1)请改正图中的错误(至少两种)① 、② 。
(2)操作步骤:
A:计算:所称取氯化钠的质量,水的体积。
B:称量:用托盘天平称量,氯化钠应放在左盘。
C:溶解:用量筒来量取所需的水(水的密度为1g/cm3),量筒的规格是 ① (从下列中选用:10mL、50 mL、100 mL);量水时,量筒必须平放,视线要跟 ② 保持水平;溶解氯化钠要用到玻璃棒,其作用是搅拌。若用自来水配制,自来水是 ③ (填“硬水”或“软水”),可以用 ④ 来检验。
D:装瓶贴签。
(3)如果配制的盐水中,NaCl的质量分数小于5%,则可能造成误差的原因有(至少举出一条) 。
(4)此题的所配溶液,也可用10%的氯化钠浓溶液 克,然后加水稀释得到。
请从氢气、氮气、氧气、一氧化碳、二氧化碳、二氧化硫等六种气体及粉尘中,按要求将相应物质的名称填写在题中的空白处:
(1)属于空气污染物的气体是。
(2)能支持燃烧的气体是。
(3)焊接金属时常用作保护气的是。
(4)绿色植物光合作用吸收的气体是。
法国化学家拉瓦锡通过实验得出的结论是氧气约占空气总体积的1/5.某同学用下图装置进行验证,
实验后发现气体减少的体积小于1/5,请你帮助这位同学找出两种可能造成这样结果的原因:
①;
② .
根据下图所示水、二氧化碳和氧气的性质实验,请回答以下问题。 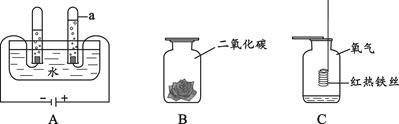
(1)仪器a的名称是。A装置中发生反应的化学方程式为。用带火星的木条检验a中的气体,观察到木条复燃,该气体是。
(2)将白色纸花用紫色石蕊试液喷湿,放入集气瓶B中,观察到的现象是。
(3)集气瓶C中的现象:铁丝在氧气中剧烈燃烧,,放出大量的热,有黑色固体生成。该反应的化学方程式为。
人们的日常生活离不开金属。
(1)地壳中含量最高的金属元素是。
(2)奥运场馆“鸟巢”使用了大量的钢铁。钢铁与直接接触容易生锈造成损失,在钢铁表面涂油、刷漆等,都能防止钢铁生锈。
(3)实验室用图示实验模拟炼铁反应的原理,回答下列问题。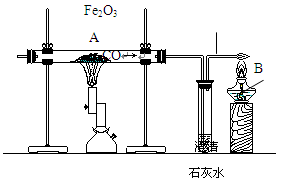
a处可观察到的现象是;b处点燃酒精灯的目的是。
(4)某校兴趣小组同学收集到含有硝酸银的溶液,他们利用铁和锌回收其中的金属银,其实验过程如图所示。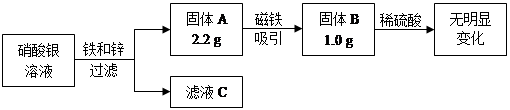
下列说法正确的是(填字母序号)。
| A.固体A中一定有银、铁,可能有锌 |
| B.固体B一定是1.0 g金属银 |
| C.滤液C中的溶质可能只有硝酸锌 |
| D.滤液C中的溶质可能是硝酸锌和硝酸亚铁 |
A和B反应生成C和D。反应前后分子变化的微观示意图如下所示。

反应前反应后
请回答以下问题:
(1)1个A分子中含有_____个氢原子。
(2)A中氮元素和氢元素的质量比为_____。
(3)4种物质中,属于化合物的是_____(填化学式)。
(4)该反应的基本反应类型为_____。
(5)在该反应中,生成C和D的质量比为_____(计算结果用最简整数比表示)。