下列各溶液中能大量共存的离子组是
| A.c(H+)=10-14 mol·L-1的溶液中:Na+、AlO2-、S2-、SO32- |
| B.使pH试纸呈红色的溶液中:Fe2+、I-、NO3-、Cl- |
| C.碳酸氢钠溶液中:K+、SO42-、Cl-、H+ |
| D.使酚酞试液呈红色的溶液中:Mg2+、Cu2+、SO42-、K+ |
金属镍有广泛的用途。粗镍中含有少量杂质Fe、Zn、Cu、Pt,可用电解法制备高纯度的镍(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是
| A.阳极发生还原反应,其电极反应:Ni2++2e-=Ni |
| B.电解过程中,阳极质量的减少与阴极质量的增加相等 |
| C.电解后,溶液中存在的阳离子只有Fe2+和Zn2+ |
| D.电解后,电解槽底部的阳极泥中只有Cu和Pt |
某小组为研究电化学原理,设计如图装置,下列叙述不正确的是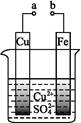
| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu |
| C.无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色 |
| D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 |
观察下列几个装置示意图,有关叙述正确的是
| A.装置①中阳极上析出红色固体 |
| B.装置②的待镀铁制品应与电源正极相连 |
| C.装置③闭合电键后,外电路电子由a极流向b极 |
| D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
| A.氯碱工业中电解饱和食盐水时,阳极的电极反应为:2Cl--2e-=Cl2↑ |
| B.氢氧燃料电池的负极反应:O2+2H2O+4e-=4OH- |
| C.粗铜精炼时,与电源正极相连的是纯铜,电极反应为:Cu-2e-=Cu2+ |
| D.钢铁发生电化学腐蚀的正极反应:Fe-2e-=Fe2+ |
下图各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是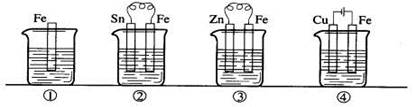
| A.④>②>①>③ | B.②>①>③>④ | C.④>②>③>① | D.③>②>④>① |