一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3=2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为
| A.5∶3 | B.5∶4 | C.1∶1 | D.3∶5 |
下列叙述中,正确的是( )
①电解池是将化学能转变成电能的装置 ②原电池是将电能转变成化学能的装置 ③金属和石墨导电均为物理变化,电解质溶液导电是化学变化 ④不能自发进行的氧化还原反应,通过电解的原理有可能实现 ⑤电镀过程相当于金属的“迁移”,可视为物理变化
| A.①②③④ | B.③④ |
| C.③④⑤ | D.④ |
下列热化学方程式中,ΔH的绝对值能表示可燃物的燃烧热的是( )
| A.C(s)+O2(g)===CO(g) ΔH=-110.5 kJ·mol-1 |
| B.CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-802.3 kJ·mol-1 |
| C.2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1 |
| D.CO(g)+O2(g)===CO2(g) ΔH=-283 kJ·mol-1 |
下列属于放热反应的是( )
| A.铝和盐酸反应 | B.焦炭和二氧化碳共热 |
| C.石灰石的分解 | D.氯化铵与氢氧化钡反应 |
将氢氧化钠溶液滴入某混有盐酸的氯化镁和氯化铝的混合溶液中,则下列图像变化趋势正确的是: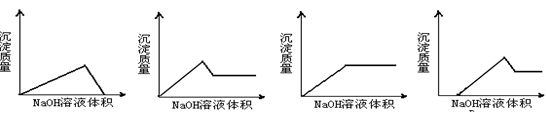
A B C D
有100 mL3mol·L-1NaOH溶液和100 mL1 mol·L-1AlCl3溶液。按如下两种方法进行实验:①将氢氧化钠溶液分多次加到AlCl3溶液中;②将AlCl3溶液分多次加到NaOH溶液中。比较两次实验结果是:
| A.现象相同,沉淀量相等 | B.现象不同,沉淀量相等 |
| C.现象相同,沉淀量不等 | D.现象不同,沉淀量不等 |