碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
(1)该反应氧化产物与还原产物质量比是_________________;
(2)先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4,振荡,这时候,观察到的现象是_________________;
(3)某学生在一次分液操作中发现上下层溶液都是无色液体,无法知道分液漏斗中的液体哪一层是有机层,哪一层是水层,请你用简单的方法帮他鉴别出来,写出有关步骤及判断方法___________________。
(4)在容量瓶的使用方法中,下列操作正确的是____________
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
D.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
(5)上面实验中用到一定物质的量浓度的稀硫酸,若配制0.5mol/L的硫酸溶液450mL,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为_________mL,如果实验室有15mL、20mL、50mL量筒,应选用___________mL量筒最好。
(6)下面操作造成所配稀硫酸溶液浓度偏高的是__________
A.溶解的时候溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
在有机物分子中,不同氢原子的核磁共振谱中给出的信号也不同,根据信号可以确定有机物分子中氢原子的种类和数目。例如二乙醚的结构简式为: CH3—CH2—O—CH2—CH3,其核磁共振谱中给出的信号有两个,如图①所示:
(1)下列物质中,其核磁共振氢谱中给出的信号只有一个的是。(填序号)
| A.CH3CH3 | B.CH3COOH | C. CH3OH | D. CH3OCH3 |
(2)化合物A和B的分子式都是C2H4Br2, A的核磁共振氢谱图如右图②所示,则A的结构简式为,请预测B的核磁共振氢谱上有种信号。
(3)在常温下测得的某烃C8H10(不能与溴水反应)的核磁共振谱上,观察到两种类型的H原子给出的信号,其强度之比为2:3,试确定该烃的结构简式为;该烃在光照下生成的一氯代物在核磁共振谱中可产生种信号,强度比为。
(4)在常温下测定相对分子质量为128的某链烃的核磁共振谱,观察到两种类型的H原子给出的信号,其强度之比为9:1,则该烃的结构简式为,其名称为。
药物Z可用于治疗哮喘、系统性红斑狼疮等,可由X(咖啡酸)和Y(1,4-环己二酮单乙二醇缩酮)为原料合成(如下图)。
试填空:
(1)X的分子式为;该分子中最多共面的碳原子数为。
(2)Y中含有个手性碳原子。
(3)Z能发生反应。(填序号)
A.取代反应 B.消去反应C.加成反应 D.催化氧化反应
(4)鉴别X和Z可用下列何种物质?
A.Br2水B.酸性KMnO4溶液C.FeCl3溶液 D.Na2CO3溶液
(5)1 mol Z与足量的氢氧化钠溶液充分反应,需要消耗氢氧化钠mol;
1 mol Z在一定条件下与足量Br2充分反应,需要消耗Br2 mol。
1 mol Z在一定条件下与足量H2充分反应,需要消耗H2 mol。
按要求填空:
(1)某有机物的结构简式为: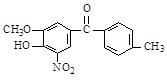 ,该有机物中含氧官能团有:、、、(写官能团名称)。
,该有机物中含氧官能团有:、、、(写官能团名称)。
(2)有机物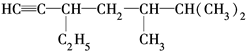 的系统名称是,将其在催化剂存在下完全氢化,所得烷烃的系统名称是。
的系统名称是,将其在催化剂存在下完全氢化,所得烷烃的系统名称是。
(3)下图是某一有机物的红外光谱图,该有机物的相对分子质量为74,则其结构简式为。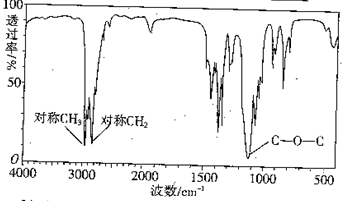
(4)苯的同系物中,有的侧链能被酸性高锰酸钾溶液氧化,生成芳香酸,反应如下: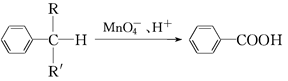
(R、R′表示烷基或氢原子)
①现有苯的同系物甲和乙,分子式都是C10H14。甲不能被酸性高锰酸钾溶液氧化为芳香酸,它的结构简式是;乙能被酸性高锰酸钾溶液氧化为分子式为C8H6O4的芳香酸,则乙可能的结构有种。
②有机物丙也是苯的同系物,分子式也是C10H14,它的苯环上的一溴代物只有一种。丙的结构简式共有四种,写出其余三种: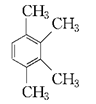 、、、。
、、、。
(5)已知:RCH=CHR,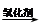 RCOOH+R,COOH。写出
RCOOH+R,COOH。写出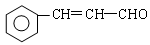 在强氧化剂条件下生成
在强氧化剂条件下生成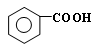 和另一种有机物(写出其结构简式)。
和另一种有机物(写出其结构简式)。
铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)
(1)硝酸在该反应中表现出的性质是_____,该反应的还原产物是_____。
(2)0.4molCu被硝酸完全溶解后,硝酸得到的电子数是_____,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是_____mol。
(3)0.3molCu被另一浓度的硝酸完全溶解后,如果此时产生的NO和NO2气体总体积在标准状况下为8.96 L,则被还原的硝酸的物质的量是_____ mol,参加反应的硝酸的物质的量是_____mol,产生的混合气体中NO和NO2体积比为_______。
(1)已知0.1mol/L的NaHSO4溶液中H+的物质的量浓度为0.1mol/L,请回答下列问题:
①写出NaHSO4在水溶液中电离的方程式:___________________________________。
②若将NaHSO4与Ba(OH)2在溶液中按物质的量比为2:1混合,反应的离子方程式是:___________________________________________________________。
若将NaHSO4与Ba(OH)2在溶液中按物质的量比为1:1混合,反应的离子方程式是:___________________________________________________________。