下列关于反应能量的说法正确的是
| A.101kPa时,H2(g)+1/2O2(g)===H2O(g) ΔH=-248kJ·mol-1,H2的燃烧热为248kJ·mol-1 |
| B.利用盖斯定律可以计算难以测量的反应热 |
| C.H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1,含1 mol NaOH的氢氧化钠的溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ的热量 |
| D.相同条件下,如果1 mol H原子所具有的能量为E1,1 mol H2所具有能量为E2,则2E1=E2 |
关于右图所示的原电池,下列说法正确的是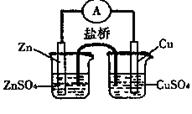
| A.电子从铜电极通过检流计流向锌电极 |
| B.盐桥中的阳离子向硫酸铜溶液中迁移 |
| C.锌电极发生还原反应,铜电极发生氧化反应 |
D.铜电极上发生的电极反应是 |
下列事实于氢键有关的是
| A.水加热到很高的温度都难以分解 | B.水结成冰体积膨胀,密度变小 |
| C.CH4、SiH4、GeH4、SnH4熔点随着相对分子质量的增大而升高 | |
| D.HF、HCl、HBr、HI的热稳定性依次减弱 |
最近科学家成功地制成了一种新型的碳氧化合物,该化合物晶体中每个碳原子均以四个共价单键与氧原子结合成为一种空间网状的无限伸展结构,下列对该晶体叙述错误的是
| A.该物质的化学式为CO4 | B.晶体的溶沸点高,硬度大 |
| C.晶体中C原子数与C-O化学键之比1:4 | D.晶体的空间最小环共由12个原子构成 |
氮化硅是一种新合成的结构材料,它是一种超硬、耐磨、耐高温的物质。下列各组物质熔化时,所克服的粒子间的作用力与氮化硅所克服的粒子间的作用力都相同的是
| A.石膏和金刚石 | B.晶体硅和水晶 |
| C.冰和干冰 | D.铝和蒽 |
下列物质的熔、沸点高低顺序正确的是
| A.金刚石>晶体硅>二氧化硅>碳化硅 | B.CI4>CBr4>CCl4>CH4 |
| C.MgO>H2O>O2>NH3 | D.金刚石>生铁>纯铁>钠 |