已知有热化学方程式:SO2(g)+ 1/2 O2(g) = SO3(g);△H =-98.32kJ/mol。现有2molSO2参加反应,当放出137.5kJ热量时,SO2的转化率最接近于
| A.40% | B.50% | C.70% | D.90% |
对于某些离子的检验及结论正确的是( )
| A.加入稀盐酸产生无色气体,将气体通入足量澄清石灰水中,溶液变浑浊,一定有CO32﹣ |
| B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42¯ |
| C.加入盐酸无现象,再加氯化钡溶液有白色沉淀生成,原溶液一定有硫酸根离子 |
| D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
对于相同质量的二氧化硫和三氧化硫,下列说法中正确的是( )
| A.含氧原子的个数比为2:3 | B.含硫原子的个数比为1:1 |
| C.含氧元素的质量比为6:5 | D.含硫元素的质量比为5:4 |
在反应2KMnO4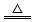 K2MnO4+MnO2+O2↑中,还原产物是()
K2MnO4+MnO2+O2↑中,还原产物是()
①KMnO4 ②K2MnO4③MnO2 ④O2
| A.①和② | B.②和③ | C.只有④ | D.只有③ |
实验室加热氯酸钾与MnO2的混合物制氧气,从剩余物中回收二氧化锰的操作顺序正确的是()
| A.溶解、过滤、蒸发、洗涤 | B.溶解、过滤、洗涤、干燥 |
| C.溶解、蒸发、洗涤、过滤 | D.溶解、洗涤、过滤、干燥 |
下列反应中,离子方程式书写正确的是( )
| A.过量CO2与澄清石灰水反应:Ca2++2OH﹣+CO2═ CaCO3↓+H2O |
| B.向KHSO4溶液中加入Ba(OH)2溶液至所得溶液的pH=7:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| C.向Ca(HCO3)2溶液中滴入过量的NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| D.硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |