下列叙述不正确的是
A,10mL质量分数为98%的H2SO4用10mL水稀释后;H2SO4的质量分数大于49%
B.配制0.1 mol·L-1的Na2CO3溶液480mL,需用500ml容量瓶
C.在标准状况下,将22.4L氨气溶于1L水中,得到1mol·L-1的氨水
D.向2等份不饱和的烧碱溶液中分别加入一定量的Na2O2和Na2O,使溶液均恰好饱和,则加入的Na2O2与Na2O的物质的量之比等于1:1(保持温度不变)
能说明苯分子苯环的平面正六边形结构中,碳碳键不是单双键交替排布的事实是
| A.苯的一元取代物没有同分异构体 |
| B.苯的邻位二元取代物只有一种 |
| C.苯的间位二元取代物只有一种 |
| D.苯的对位二元取代物只有一种 |
某溶液含有较多的Na2SO4和少量的Fe2(SO4)3。若用该溶液制取芒硝,可供选择的操作有:①加适量的H2SO4溶液,②加金属Na,③结晶,④加过量的NaOH溶液,⑤加强热脱结晶水,⑥过滤。正确的操作步骤是
| A.②⑥③ |
| B.④⑥①③ |
| C.④⑥③⑤ |
| D.②⑥①③⑤ |
有一种碘和氧的化合物可以称为碘酸碘,其中碘元素呈+ 3、+ 5两种价态,这种化合物的化学式是
| A.I2O4 |
| B.I3O5 |
| C.I4O7 |
| D.I4O9 |
下列离子方程式中正确的是
| A.在氯化铝溶液中加入过量氨水 Al3++3OH-=Al(OH)3↓ |
B.在硫酸铜溶液中加入过量氢氧化钡溶液 |
C.在澄清石灰水中通入过量二氧化碳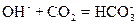 |
| D.在碳酸氢钙溶液中加入过量氢氧化钠溶液 |
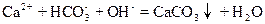
下面有关晶体的叙述中,不正确的是
| A.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子 |
| B.氯化钠晶体中,每个Na+周围距离相等的Na+共有6个 |
| C.氯化铯晶体中,每个Cs+周围紧邻8个Cl- |
| D.干冰晶体中,每个CO2分子周围紧邻10个CO2分子 |