下列物质的分子中既有σ键,又有π键的是
①HCl②H2O③N2④H2O2⑤C2H4⑥C2H2
| A.①②③ | B.③④⑤⑥ | C.③⑤⑥ | D.①③⑥ |
在100mL混合溶液中,HNO3和H2SO4物质的量浓度分别为0.4mol/L和0.1mol/L,向该溶液中加入1.92g铜粉,加热,待充分反应后,所得溶液中Cu2+物质的量浓度(mol/L)为 ()
| A.0.15 | B.0.20 | C.0.225 | D.0.45 |
短周期金属元素甲~戊在元素周期表中的相对位置如下表所示,下面判断正确的是
| 甲 |
乙 |
|||||
| 丙 |
丁 |
戊
|
NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,22.4L二氯甲烷的分子数约为NA个 |
| B.1.7g H2O2中含有的电子数为0.9 NA |
| C.1mol Na2O2固体中含离子总数为4 NA . |
| D.电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g |
如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。其它条件相同时,在Ⅰ、Ⅱ中分别加入2molX和2molY,起始时容器体积均为VL,发生如下反应并达到平衡(X、Y状态未知):2X(?) + Y(?)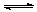 aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是
aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是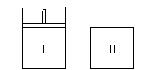
| A.若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ |
| B.若X、Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ |
| C.若X为固态,Y为气态,则Ⅰ、Ⅱ中从起始到平衡所需时间Ⅰ>Ⅱ |
| D.平衡时Ⅰ容器的体积小于VL |
在密闭容器中,对于可逆反应A+3B  2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是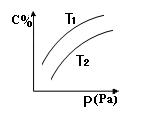
| A.A一定为气体 |
| B.B一定为气体 |
| C.该反应是放热反应 |
| D.若正反应方向△H <0,则T1>T 2 |